Обратимое растворение
Cтраница 1
Обратимое растворение сводится к образованию сольватов на поверхности реагирующей твердой фазы и переносу их в раствор. Обратимость этого процесса заключается в том, что полученный раствор можно кристаллизацией разделить на исходные реагенты. Очевидным примером такого процесса является растворение ионных кристаллов в воде с образованием гидратированных ионов. [1]
Таким образом, обратимое растворение металла с поверхности вращающегося дискового электрода также описывается поляризационной кривой с максимумом тока, величина которого прямо пропорциональна количеству металла на электроде или в соответствии с формулой ( 11 1) концентрации его ионов в растворе. [2]
Коррозия, вызываемая жидкими металлами и расплавами, может быть простым обратимым растворением ( с переносом вещества или без него), или избирательным растворением отдельных компонентов; кроме того, она может быть местной. [3]
Лиофильные коллоиды, выделенные из дисперсионной среды, при повторном внесении в нее возвращаются из состояния студня в состояние золя. Обратимое растворение может быть вызвано даже у необратимых коллоидов, если их соединить с обратимыми. Такой золь серебра можно путем выпаривания превратить в твердый продукт, который обладает способностью снова растворяться в воде, образуя золь. Вследствие того защитного действия, которое в подобных случаях оказывают обратимые коллоиды, повышая стабильность необратимых, их называют защитными коллоидами. При применении защитных коллоидов золи могут быть получены с более высокими концентрациями, чем обычно. Примером концентрированного золя, получаемого с применением защитного коллоида, является медицинский препарат колларгол, содержащий свыше 70 % серебра. [4]
Лиофильные коллоиды, выделившиеся из дисперсной среды, при повторном внесении в нее возвращаются из состояния студня в состояние золя. Обратимое растворение может быть вызвано даже у необратимых коллоидов, если их соединить с обратимыми. Например, если прибавить к раствору соли серебра небольшое количество желатины, белка или некоторых продуктов распада его и восстановить серебро до образования золя, то степень дисперсности коллоидного серебра в этих условиях получения оказывается более высокой и золь менее подвержен влияниям факторов, вызывающих коагуляцию. Золь серебра можно путем выпаривания превратить в твердый продукт, который обладает способностью снова растворяться в воде, образуя золь. Вследствие того защитного действия, которое в подобных случаях оказывают обратимые коллоиды, повышая стабильность необратимых, их называют защитными коллоидами. При применении защитных коллоидов золи могут быть получены с более высокими концентрациями, чем обычно. Примером концентрированного золя, получаемого с применением защитного коллоида, является медицинский препарат колларгол, содержащий свыше 70 % серебра. [5]
Процессы растворения могут идти как в диффузионной, так и в кинетической области. При физическом обратимом растворении происходит разрушение кристаллической решетки и переход частиц твердого вещества в раствор. Чем мельче кристаллы, тем больше их удельная поверхность и тем интенсивнее идет растворение. Кроме того, в этом случае идет более интенсивное разрушение кристаллической решетки, так как в мелких кристаллах относительная доля ионов и молекул, находящаяся у ребер и вершин, больше, чем в крупных. По этим причинам мелкие кристаллы растворяются быстрее крупных, имеющих развитые грани. [6]
Реакции, сводящиеся к образованию сольватов на поверхности и последующему переносу их в раствор. По своему типу эти реакции могут быть сходны с теми, которые наблюдаются при обратимом растворении. [7]
Кинетика взаимодействия в системе Ж - Т рассматривается на примере процессов растворения и выщелачивания. Обычно процессы растворения идут в диффузионной или переходной области. При физическом обратимом растворении разрушается кристаллическая решетка и частицы твердого вещества переходят в раствор. [8]
Кинетика взаимодействия в системе Ж - Т рассмотрена на примере процессов растворения и выщелачивания. Обычно процессы растворения идут в диффузионной или переходной области. При физическом обратимом растворении происходит разрушение кристаллической решетки и переход частиц твердого вещества в раствор. [9]
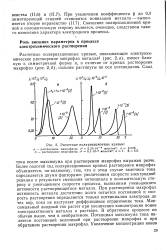 |
Расчетные поляризационные кривые. [10] |
Более пологий ход поляризационных кривых растворения микрофаз объясняется, по-видимому, тем, что в этом случае величина тока определяется двумя факторами: увеличением скорости электродной реакции в результате смещения потенциала в положительную сторону и уменьшением скорости процесса, вызванным уменьшением активности растворяющегося металла. При растворении макрофаз активность металла достаточно долго остается постоянной и скорость растворения определяется только потенциалом электрода до тех пор, пока не наступает диффузионное ограничение тока. Максимальный анодный ток растет при увеличении концентрации ионов электроактивного металла в растворе. В обратимом процессе он обычно выше, чем в необратимом. Потенциал максимума тока является постоянной величиной при растворении микрофаз и при обратимом растворении макрофаз. [11]
Страницы: 1