Анодное растворение - марганец
Cтраница 1
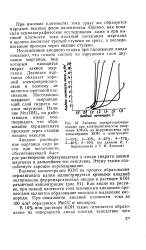 |
Анодные поляризационные кривые при электролитическом получении КМпО4 из ферромарганца при концентрации КОН в электролите. [1] |
Анодное растворение марганца надо вести при щелочности, обеспечивающей быстрое растворение образующегося у анода гидрата закиси марганца и дальнейшее его окисление. Этому также способствует хорошее перемешивание. [2]
Механизм анодного растворения марганца с образованием перманганата - довольно сложный. [3]
Для понимания механизма анодного растворения марганца необходимо определение точных значений анодных потенциалов, измерение которых обычным путем вследствие образования пассивирующих пленок не дает достоверные результаты. Получение более точных анодных потенциалов возможно: а) путем непрерывного удаления пассивирующей пленки с анода в процессе измерения; б) проведением измерений в условиях, задерживающих образование пассивирующей пленки; в) настолько быстрыми измерениями, что поверхность анода успевает лишь незначительна измениться. [4]
Существует две точки зрения на механизм анодного растворения марганца. Согласно одной из них при анодном растворении непосредственно образуются ионы манганита и перманганата. В соответствии с другой точкой зрения окисление марганца происходит через промежуточные степени окисления. Результаты исследований показывают, что наиболее вероятен последний механизм окисления марганца. [5]
Из уравнения видно, что скорость анодного растворения марганца в таких растворах при постоянном потенциале закономерно снижается с ростом содержания кислоты. Наиболее вероятно, что ингибирующее действие кислоты обусловлено протеканием химической реакции, продуктом которой являются ионы водорода и которая предшествует лимитирующей реакции ионизации марганца. [6]
Существуют две точки зрения на механизм анодного растворения марганца. [7]
 |
Поляризационные кривые при янпдном растворении марганца в щелочи, [ NaOH ] 400 г / л. [8] |
Некоторые исследователи считают, что при анодном растворении марганца в щелочах он переходит в раствор непосредственно в шести - или семивалентной форме. Другие предполагают последовательное окисление. [9]
Данный метод получения перманганата калия основан на анодном растворении марганца из сплавов. [10]
Некоторые исследователи утверждают [2], что при анодном растворении марганца в щелочах он переходит в раствор непосредственно в виде шести - или семивалентной формы, другие [3] говорят о последовательном окислении. Анодное растворение марганца и его сплавов в щелочах сопровождается сильной пассивацией анодов, что затрудняет осуществление технологического процесса получения перманганата. [11]
Существуют два электрохимических метода синтеза перманганата - анодное окисление манганата и анодное растворение марганца и его сплавов. [12]
Концентрация гидроксида калия в растворе электролита оказывает существенное влияние на процесс анодного растворения марганца. С одной стороны она должна обеспечивать активное растворение марганца и не приводить к растворению железа из ферромарганцевого анода. Добавление в раствор до 3 - 5 % Na2SiO3 уменьшает количество диоксида марганца в шламе и устраняет пассивацию анода. [13]
Запатентован [37, 38] способ получения ценного антидетонатора - карбонила циклопентадиенилмарганца, основанный на анодном растворении марганца. В диметилформамиде растворяют ди-мер метилциклопентадиена, пентакарбонил железа и хлорид марганца. При этом с выходом по току - 7 % получают трикарбонилметилциклопентадиенилмарганец. [14]
 |
Поляризационные кривые при анодном растворении марганца в щелочи ( NaOH 400 г / л. [15] |
Страницы: 1 2