Анодное растворение - сплав
Cтраница 3
В рассматриваемом аспекте наиболее изучены коррозия и анодное растворение сплавов системы Zn - Си, в которой образуется несколько промежуточных фаз с достаточно широкой областью гомогенности. [31]
 |
Потснциодпнамические кривые. / - реальная. 2 - идеальная. [32] |
После окончания коррозионных испытаний и опытов по анодному растворению сплавов капли ртути визуально обнаруживались на образцах. [33]
С увеличением концентрации кислоты на анодных поляризационных кривых фиксируется петля анодного растворения сплава. [34]
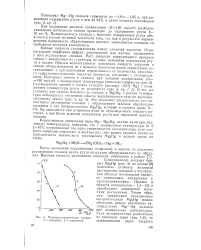
Процесс экстрагивной коррозии может наблюдаться как при наложении внешнего тока вследствие анодного растворения сплава, так и за счет тока, создаваемого окислительно-восстановительной системой, присутствующей в растворе. Явление экстрагивной коррозии может быть объяснено с помощью дифференциальных анодных кривых и поляризационных диаграмм ( фиг. [35]
Исследованиями, проведенными М. Н. Орфановой, выявлено, что характер влияния присутствующих в промывочной жидкости анионов на процесс анодного растворения сплава Д16Т зависит от характера их воздействия на поверхность груб. [36]
Цель работы состоит в определении потенциала растворения сплава и распределении составляющих сплава между раствором и шламом при анодном растворении сплава Sn-Bi в зависимости от его состава. [37]
В случае невозможности увеличить поверхность анодов следует применять подвижные ( или вращающиеся) аноды, что позволяет улучшить анодное растворение сплава. Перемешивание электролита воздухом с целью улучшения анодного поведения сплава не рекомендуется в связи с повышенным переходом двухвалентного олова в четырехвалентное. [38]
 |
Схема, показывающая изменение во времени емкостного / 0 и фа-радеевского / ф токов при поляризации электрода прямоугольным напряжением. [39] |
Поэтому применение прямоугольного поляризующего тока очень удобно для изучения реакций весстановления, которые имеют место при катодной поляризации после предварительного анодного растворения сплава. [40]
Следует отметить, что на основании недавних исследований [ 311 при растворении твердых растворов и даже гетерогенных сплавов не всегда можно представить анодное растворение сплава рядом парциальных кривых, соответствующих растворению отдельных структурных составляющих. В общем случае при рассмотрении парциальных кривых нужно учитывать взаимное влияние компонентов. Так, например, при растворении сплавов Fe-Сг в кислых растворах [32] было установлено, что по характеру зависимости парциальных скоростей растворения железа и хрома от потенциала и рН в активной области сплавы можно разделить на две группы. Для сплавов с низким содержанием хрома каждая структурная составляющая характеризуется парциальными поляризационными кривыми, совпадающими по кинетическим параметрам с чистым железом. [41]
В процессе электролиза с анодами из двойных сплавов Мп - Fe при температуре электролита 18 - 20 С, содержащего ( в г / л): К2МпО4 - 113 5; КМпО4 - 76 5; КОН-1148 и К2СО3 - 75 9, снижается доля перманганата, образующего вследствие анодного растворения сплава при увеличении в нем содержания железа. Соответственно увеличивается доля перманганата, образующегося в результате анодного окисления манганата. [42]
Аналогичное объяснение можно дать более высокой коррозионной стойкости сплава Ti - 15 % Mo - 0 1 % Pd no сравнению со сплавом Ti - 15 % Сг - 0, 1 % Pd и сплавом Ti - 0 1 % Pd в 10 % - ном растворе кипящей токи анодного растворения сплавов Ti - 15 % Mo, Ti - 15 % Сг и нелегированного титана при стационарных потенциалах этих сплавов, которые имеют близкие значения ( фиг. [43]
В процессе электролиза с анодами из двойных сплавов марганца с железом при температуре 18 - 20 С электролита, содержащего 113 5 г / л КаМпО4, 16 5 г / л КМпО4, 114 8 г / л КОН и 75 9 г / л К2СО3, снижается доля перманганата, образующегося вследствие анодного растворения сплава с ростом содержания в нем железа. Соответственно увеличивается доля перманганата, образующегося в результате анодного окисления манганата. [44]
Однако это не единственная причина, которая ограничивает время анодной поляризации в этих исследованиях. Анодное растворение сплавов, имеющих высокое содержание неблагородного компонента, происходит при столь отрицательных потенциалах, что в период анодной поляризации оказывается возможным восстановление на поверхности исследуемого электрода ионов благородного металла. Такое восстановление происходит не сразу после начала анодной поляризации сплава, а через некоторое время, когда в приэлектродном слое будет достигнута необходимая концентрация ионов благородного компонента для преодоления торможений образования первых зародышей новой фазы. Поэтому сокращение времени анодной поляризации приводит к предупреждению обратного осаждения на исследуемом электроде благородного компонента. В этом случае необходимо перейти к поляризации с высокой частотой изменения полярности, или, собственно говоря, к поляризации переменным током. [45]
Страницы: 1 2 3 4 5