Растворимость - известь
Cтраница 1
Растворимость извести в воде невелика и понижается с повышением температуры. [1]
Повышение растворимости извести путем увеличения ее дисперсности в ряде случаев имеет не меньшее значение, чем измельчение песка. Опыты показывают, что, увеличивая дисперсность Са ( ОН) 2, можно повысить прочность автоклавных силикатных изделий. [2]
При обычных температурах растворимость извести значительно выше растворимости кремнезема. При повышении температуры растворимость извести падает, а растворимость кремнезема возрастает. Растворимость аморфной кремнекислоты уже при температуре выше 403 К становится больше растворимости Са ( ОН) 2, а при 473 К превышает ее более чем в 15 раз. Растворимость крупнокристаллического кварца сравнивается с растворимостью Са ( ОН) 2 при температуре 443 - 453 К, а при 473 К превышает ее в 4 5 раза. [3]
При обычных температурах растворимость извести значительно выше растворимости кремнезема. При повышении температуры растворимость извести падает, а растворимость кремнезема возрастает. Растворимость аморфной кремнекислоты уже при температуре выше 130 С становится больше растворимости Са ( ОН) 2, а при 200 С превышает ее более чем в 15 раз. Растворимость крупнокристаллического кварца при температуре 170 - 180 С становится такой же, как и растворимость Са ( ОН) 2, а при 200 С превышает ее в 4 5 раза. [4]
Известно, что растворимость извести в растворе соли выше, чем в дистиллированной воде. Максимальная растворимость гидроксида кальция наблюдается в растворе, содержащем 60 г / л NaCl. Следовательно, раствор NaCl должен быть более агрессивным, чем дистиллированная вода. Однако избыток кремнезема в шлакопесчаных цементах при повышенных температурах активно связывает известь и, как показали настоящие исследования ( см. табл. 12.3), выщелачивающее воздействие NaCl на цементы ШПЦС-120 и ШПЦС-200 проявляется незначительно, вследствие чего непрерывно растет прочность. У чистого шлака, твердевшего как в растворе NaCl, так и в дистиллированной воде, к трехмесячному сроку содержание СаО по сравнению с исходным образцом снижается в первом случае на 12 63 %, во втором - на 5 62 %, причем наблюдается непрерывный процесс выщелачивания извести. Указанные изменения физико-механических характеристик камня на основе макеевского основного шлака подтверждаются данными рентгенофазовых и термических исследований. [5]
 |
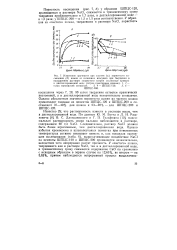
Растворимость извести в воде. [6] |
В связи с малой растворимостью извести в воде ее часто дозируют в воду не в виде раствора, а в виде суспензии, называемой известковым молоком, концентрация СаО в котором может достигать 10 - Ii5 % по весу. [7]
Хлористый натрий несколько повышает растворимость извести, поэтому минерализованные воды, содержащие эту соль, обладают более высокой выщелачивающей способностью, чем простые. [8]
Известно [5], что растворимость извести в растворе выше, чем в дистиллированной воде. По данным Ю. М. Бутта и Л. Н. Раш-ковича i [8], В. С. Данюшевского и Г. П. Гельфмана [12], максимальная растворимость окиси кальция наблюдается в растворе, содержащем 60 г / л NaCl. Следовательно, раствор NaCl должен быть более агрессивным, чем дистиллированная вода. Однако избыток кремнезема в шлакопесчаных цементах при повышенных температурах активно связывает известь и, как показали настоящие исследования ( табл. 6), выщелачивающее воздействие NaCl на цементы ШПЦС-120 и ШПЦС-200 проявляется незначительно, вследствие чего непрерывно растет прочность. [10]
Хлорид натрия сильно повышает растворимость извести, поэтому минерализованные воды, содержащие эту соль, обладают более высокой выщелачивающей способностью, чем пресные. [11]
При низких положительных температурах растворимость извести повышается, поэтому можно полагать, что это и является причиной большей эффективности добавки СаСЬ и НС1 при этих температурах. [12]
Щелочь добавляется для снижения растворимости извести. Кроме того, присутствие щелочи в известковом растворе активизирует процессы, усиливает действие реагентов - понизителей вязкости и водоотдачи. [13]
Весьма интересно указание Ловица о растворимости титановой извести ( окислов титана) в сильных кислотах. Известно, чтс двуокись титана нерастворима в крепких кислотах, тогда как гидрат окиси Ti ( OH) 4 оказывается хорошо растворимым. Иначе говоря, он установил кислые свойства этих окислов. [14]
Фергусон и Мервин обнаружили небольшую, но отчетливую растворимость извести и кремнезема в обеих модификациях метасиликата кальция. [15]
Страницы: 1 2 3 4