Растворимость - хлористое серебро
Cтраница 1
Растворимость хлористого серебра настолько мала, что при добавлении избытка раствора хлористого натрия к раствору нитрата серебра хлористое серебро осаждается практически полностью. [1]
Вычислите произведение растворимости хлористого серебра, допускай, что активности и концентрация ионов раьны. [2]
Видно, что растворимость хлористого серебра практически не изменилась, что объясняется очень малой растворимостью цианида серебра. [3]
Рассмотрим, например, растворимость хлористого серебра в водных растнорах азотной кислоты при 25 С и атмосферном давлении. [4]
Качественные опыты показали, что растворимость свежеприготовленного хлористого серебра увеличивается в присутствии амидокомплексов платины. Однако было установлено, что при растворении хлористого серебра в растворах амидокомплексов происходит изменение твердой фазы вследствие увлечения комплекса в осадок. [5]
Абсолютно нерастворимых веществ нет, но растворимость хлористого серебра AgCl в воде так незначительна, что практически хлористое серебро принимают за нерастворимую соль. [6]
Абсолютно нерастворимых веществ нет, но растворимость хлористого серебра AgCl в воде так незначительна, что практически его принимают за нерастворимую соль. [7]
Андерсон [2] тщательно изучил элемен. Были внесены поправки на растворимость хлористого серебра и на другие факторы. [8]
Метод основан на титровании водной вытяжки азотнокислым серебром в присутствии хромовокислого калия. Сущность этого метода состоит в том, что растворимость хлористого серебра значительно меньше, чем хромовокислого серебра. При действии азотнокислого серебра на содержащую хлор водную вытяжку выпадает белый створаживающийся осадок хлористого серебра. По окончании реакции с хлором начинается взаимодействие азотнокислого серебра с хромовокислым калием в результате чего образуется хромовокислое серебро, которое имеет красно-бурый цвет. Этот момент указывает на полное связывание CV азотнокислым серебром; по количеству его, пошедшему на связывание хлор-ионов, судят о содержании последних в вытяжке. [9]
Метод основан на титровании водной вытяжки азотнокислым серебром в присутствии хромовокислого калия. Сущность этого метода состоит в том, что растворимость хлористого серебра значительно меньше, чем хромовокислого серебра. [10]
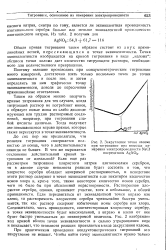 |
Закругление точки излома при титровании при помощи измерения электропроводности NaCl посредством AgNO3. [11] |
Растворенное хлористое серебро, однако, принимает участие, хотя и небольшое, в общей проводимости. Если передвигаться от эквивалентной точки вправо или влево, то растворимость хлористого серебра чрезвычайно быстро уменьшится, так как раствор содержит избыточные ионы серебра или хлора. Следовательно, часть проводимости, соответствующая хлористому серебру, в точке эквивалентности будет максимальной, а вправо и влево от нее будет быстро уменьшаться до неизмеримой величины. [12]
Вычислено из опытных значений электродвижущих сил. Андерсон [2] тщательно изучил элемент На I HC1 ( m) AgCl-Ag, содержащий соляную кислоту с концентрациями 0 00002 - О ООЗМ. Были внесены нонраикн на растворимость хлористого серебра ц на другие факторы. Эти величины очень хорошо совпадают со значениями, приведенными в таблице и полученными с помощью экстраполяции. [13]
Так как аС1 - будет при этом больше, [ чем соответствующее значение в растворе, не содержащем избытка иона хлора, то величина aAg которая определяется у равнением ( И 2) будет в этом случае меньше. Таким образом, в первом приближении на основании уравнения ( 113) можно сделать следующий вывод: в насыщенном растворе хлористого серебра, содержащем избыток ионов хлора, который обусловлен, например, присутствием в растворе хлористого калия, концентрация ионов серебра будет меньше, чем в насыщенном растворе хлористого серебра в чистой воде. Поскольку растворенное хлористое серебро можно считать полностью диссоциированным, концентрация ионов серебра является мерой растворимости соли; следовательно, растворимость хлористого серебра в присутствии избытка ионов хлора меньше, чем в чистой воде. Если не происходит образования комплексных ионов, нарушающего равновесие ( ср. [14]
Вещество сплавляют в микробомбе со смесью нитрата калия, перекиси натрия и сахара. Образующиеся галоидные соединения осаждают нитратом серебра и взвешивают. По инструкции ASTM D-1303-55 для определения хлора в полимерах и сополимерах винилхлорида [7] хлор осаждают в виде хлорида серебра стандартным раствором азотнокислого серебра. Избыток азотнокислого серебра определяют титрованием стандартным раствором тиоцианата, используя нитрат железа ( Ш) в качестве индикатора и нитробензол для понижения растворимости хлористого серебра. [15]
Страницы: 1