Растворимость - сульфат - медь
Cтраница 1
Растворимость сульфата меди при 20 С составляет 20 5 г безводной соли в 100 г воды. Сколько кристаллогидрата CuS04 5Н2О необходимо растворить при такой же температуре в 100 г воды, чтобы образовался насыщенный раствор. [1]
Растворимость сульфата меди при 20 С составляет 17 2 г на 100 г раствора. Сколько необходимо взять воды для растворения 20 г медного купороса. [2]
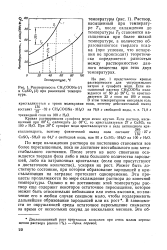 |
Растворимость CH3COONa ( / и CuSO4 ( 2 при различной температуре. [3] |
Кривая растворимости сульфата меди менее крутая. Если раствор, насыщенный при 80 С, охлаждать до 38 С, то кристаллизуется 27 г CuSO4 на 100 г ЬЬО. [4]
 |
Влияние концентрации серной кислоты на растворимость CuSO4 в воде. [5] |
На рис. 5 показано влияние концентрации серной кислоты на растворимость сульфата меди в воде. [6]
Большое накопление металлов первой группы в электролите может существенно расстроить ход электролиза. Значительные количества сульфатов железа, никеля, кобальта и цинка в растворе снижают растворимость сульфата меди, вследствие чего электролит может оказаться пересыщенным по основному металлу, и сульфат меди, станет выпадать в осадок. [7]
Большое накопление металлов первой группы в электролите может существенно расстроить ход электролиза. Значительные количества сульфатов железа, никеля, кобальта и цинка в растворе снижают растворимость сульфата меди, вследствие чего электролит может оказаться пересыщенным по основному металлу, и сульфат меди станет выпадать в осадок. [8]
Большое накопление металлов первой группы в электролите может существенно нарушить ход электролиза. Значительные количества сульфатов железа, никеля, кобальта и цинка в растворе снижают растворимость сульфата меди, вследствие чего электролит может оказаться пересыщенным по основному металлу, и сульфат меди станет выпадать в осадок. [9]
Для повышения качества покрытия концентрацию ионов меди в таких электролитах необходимо поддерживать в пределах 60 - 70 г / л, кроме того следует применять перемешивание, температура раствора должна быть низкой. Серная кислота служит для обеспечения необходимой электропроводности, но с увеличением ее концентрации понижается растворимость сульфата меди. Скорость осаждения меди в сернокислых электролитах составляет ( iK 5 А / дм2) - 1 мкм / мин. Поэтому эти электролиты позволяют меднить детали простой конфигурации. Однако сернокислые электролиты имеют лучшую выравнивающую способность, чем цианистые. Выравнивающую способность последних повышают за счет применения реверса. [10]
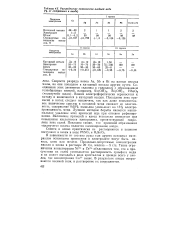 |
Распределение компонентов анодной меди ( % от содержания в аноде. [11] |
В зависимости от состава руды или других исходных материалов основными примесями в электролите могут быть никель, цинк или железо. Такие ограничения концентрации Ni2 и Zn2 объясняются тем, что в присутствии их солей уменьшается растворимость сульфата меди и он может выпадать в виде кристаллов и прежде всего у анодов, где концентрация Си2 выше. В результате аноды покрываются пленкой соли, и растворение их затрудняется. [12]
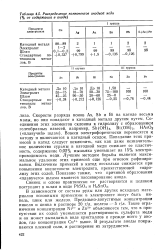 |
Распределение компонентов анодной меди ( % от содержания в аноде. [13] |
В зависимости от состава руды или других исходных материалов основными примесями в электролите могут быть никель, цинк или железо. Такие ограничения концентрации № 2 и Zn2 объясняются тем, что в присутствии их солей уменьшается растворимость сульфата меди и он может выпадать в виде кристаллов и прежде всего у анодов, где концентрация Си2 выше. В результате аноды покрываются пленкой соли, и растворение их затрудняется. [14]
Поэтому процесс осуществляют в подкисленном серной кислотой растворе. Кроме того, серная кислота повышает электропроводность электролита и снижает активность меди в нем, способствуя образованию мелкокристаллических осадков; однако с понижением рН заметно падает растворимость сульфата меди, что также следует иметь в виду. [15]
Страницы: 1 2