Растворимость - хлорид - калий
Cтраница 2
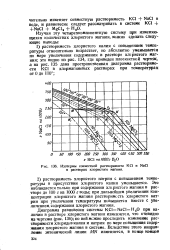 |
Изотермы совместной растворимости КС1 и NaCl в растворах хлористого магния. [16] |
Диаграмма равновесия системы КС1 - NaCl - Н2О при наличии в растворе хлористого магния изменяется, что очевидно 43 чертежа ( рис. 136); по ней можно проследить изменение растворимости хлоридов калия и натрия по мере повышения содержания хлористого магния в системе. [17]
Растворимость RbCl в органических содержание нс1 % насе ] растворителях невысокая, например в метиловом спирте 1 41 % ( при 15 С), в этиловом спирте - 0 08 % ( при 25 С), но заметно выше, чем растворимость хлорида калия, что можно использовать для их разделения. [18]
Разделение хлоридов калия и натрия, содержащихся в сильвините, основано на различной растворимости этих солей при разной температуре. Растворимость хлорида калия в воде при повышении температуры резко возрастает, в то время как растворимость хлорида натрия изменяется незначительно. В результате охлаждения раствора сильвинита из него кристаллизуется хлорид калия, а маточный раствор остается насыщенным по отношению к хлориду натрия. Дальнейшая обработка сильвинита горячим маточным раствором приводит к тому, что в него переходит хлорид калия, а в остатке содержится хлорид натрия. [19]
Очевидно образование контакта между пузырьком и частицей определяет процесс флотации. Существенное увеличение растворимости хлорида калия выше 35 С приводит к высаливанию октадециламина из раствора. [21]
Первый метод используется шире. При нормальной температуре растворимость хлоридов калия и натрия почти одинакова. С повышением температуры растворимость NaCl почти не меняется, а растворимость КС1 сильно возрастает. На холоде готовят насыщенный раствор обеих солей, затем его нагревают и обрабатывают им сильвинит. При этом раствор дополнительно насыщается хлористым калием, а часть поваренной соли вытесняется из раствора, выпадает в осадок и отделяется фильтрованием. Раствор охлаждают, и из него выкристаллизовывается избыточный хлористый калин. Кристаллы отделяют на центрифугах и сушат, а маточный раствор идет на обработку новой порции сильвинита. [22]
Первый метод используется шире. При нормальной температуре растворимость хлоридов калия и натрия почти одинакова. С повышением температуры растворимость NaCl почти не меняется, а растворимость КС1 сильно возрастает. На холоде готовят насыщенный раствор обеих солей, затем его нагревают и обрабатывают им сильвинит. При этом раствор дополнительно насыщается хлористым калием, а часть поваренной соли вытесняется из раствора, выпадает в осадок и отделяется фильтрованием. Раствор охлаждают, и из него выкристаллизовывается избыточный хлористый калий. Кристаллы отделяют на центрифугах и сушат, а маточный раствор идет на обработку новой порции сильвинита. [23]
При низкой температуре хлориды натрия и калия обладают почти одинаковой растворимостью. С повышением температуры растворимость хлорида калия возрастает существенно, а растворимость хлорида натрия - незначительно. [24]
Метод растворения и раздельной кристаллизации основан на различной растворимости в воде КС1 и NaCl при температурах 20 - 25 и 90 - 100 С. В табл. Х-2 приведена растворимость хлоридов калия и натрия при этих температурах. [25]
Переработка сильвинитовых руд методом растворения и раздельной кристаллизации основана на различной растворимости в воде КС1 и NaCl при температурах 20 - 25 и 90 - 100 С. В табл. IX2 приведена растворимость хлоридов калия и натрия при этих температурах. [26]
Данные, характеризующие растворимость хлоридов калия и натрия в зависимости от температуры, представлены на рис. 43 в виде графика. Из рисунка видно, что растворимость хлорида калия с повышением температуры резко возрастает. [27]
Производство хлористого калия из сильвинитовых руд методом растворения и раздельной кристаллизации основано на отделении КС1 от NaCl, имеющих различную растворимость в воде при температурах 20 - 25 и 90 - 100 С. В табл. 48 приведены данные о растворимости хлоридов калия и натрия при указанных температурах. [28]
Изучение изотерм тройной системы LiCl - КС1 - Н2О при 0 25, 50, 75 и 100 показало [6], что они также относятся к простым эвтониче-ским, с высаливанием хлоридом лития хлорида калия, но это действие оказалось значительно меньше, чем по отношению к сульфату лития, и, кроме того, с ростом температуры оно понижалось. При этом отмечено, что вблизи эвтонических точек растворимость хлорида калия заметно увеличивается с повышением температуры. Последнее, очевидно, связано со склонностью компонентов системы, в частности хлорида лития, к комплексообразованию, проявляющемуся только в жидкой фазе. [29]
Растворимость хлорида калия с повышением температуры значительно увеличивается а растворимость хлорида натрия незначительно уменьшается. Поэтому при охлаждении горячего насыщенного раствора ввиду понижения растворимости хлорида калия эта соль выпадает в осадок. Если этот охлажденный раствор, называемый щелоком - снова нагреть и привести в соприкосновение с сильвинитом, то растворится в нем только хлорид калия, так как раствор уже насыщен хлоридом натрия. При его охлаждении выпадает опять только хлорид калия. Таким образом, изменяя температуру раствора для выделения хлорида калия из сильвинита, можно применять один и тот же раствор, осуществляя его циркуляцию. [30]
Страницы: 1 2 3