Протолитические растворитель
Cтраница 1
Протолитические растворители могут присоединять протоны, но способность отдавать протоны выражена у них значительно сильнее. [1]
Протолитические растворители участвуют в кислотно-основном процессе. К ним относятся все растворители, не входящие в первую группу. [2]
Протолитические растворители - это химические соединения, молекулы которых способны отдавать или присоединять протоны. Протолитические растворители принимают непосредственное участие в кислотно-основном взаимодействии. К ним относятся все растворители, не входящие в первую группу. [3]
Протолитические растворители участвуют в кислотно-основном процессе. К ним относятся все растворители, не входящие в первую группу. [4]
Протолитические растворители - это химические соединения, молекулы которых способны отдавать или присоединять протоны. Протолитические растворители принимают непосредственное участие в кислотно-основном взаимодействии. К ним относятся все растворители, не входящие в первую группу. [5]
Протолитические растворители делятся на три группы: 1) кислотные, или протогенные; 2) основные, или протофильные, 3) ам-фипротные, или амфотерные. [6]
Наиболее существенное влияние на силу электролитов оказывают протолитические растворители, участвующие в протоли-тическом взаимодействии с растворенным веществом. [7]
Протолитические растворители - это химические соединения, молекулы которых способны отдавать или присоединять протоны. Протолитические растворители принимают непосредственное участие в кислотно-основном взаимодействии. К ним относятся все растворители, не входящие в первую группу. [8]
Протолитические растворители - это химические соединения, молекулы которых способны отдавать или присоединять протоны. Протолитические растворители принимают непосредственное участие в кислотно-основном взаимодействии. К ним относятся все растворители, не входящие в первую группу. [9]
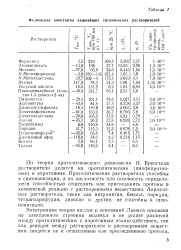 |
Физические константы важнейших органических растворителей. [10] |
Бренстеда растворители делятся на протолитические ( амофипротоы-ные) и апротонные, Протолитические растворители способны к самоионизации, а их кислотность или основность определяются способностью отщеплять или присоединять протоны в химической реакции с растворенными веществами. Апротонные растворители, такие как нитрометан, бензол, пиридин, тетрагидрофуран, диоксан и другие, не способны к самоионизации. [11]
 |
Физические константы важнейших органических растворителей. [12] |
Бренстеда растворители делятся на протолитические ( амофипротон-ные) и апротонные, Протолитические растворители способны к самоионизаци И, а их кислотность или основность определяются способностью отщеплять или присоединять протоны в химической реакции с растворенными веществами. Апротонные растворители, такие как нитрометан, бензол, пиридин, тетрагидрофуран, диоксан и другие, не способны к самоионизации. [13]
Апро-тонные растворители, например бензол, толуол, гексан, четырех-хлористый углерод, хлороформ и др., имеют обычно низкие зна-чения диэлектрической проницаемости, что благоприятствует ассоциации молекул и ионов растворенных в них веществ. Протолитические растворители, например спирты, кетоны, эфиры и др., характеризуются способностью их молекул отдавать или присоединять протоны. [14]
По характеру участия в кислотно-основном процессе все растворители подразделяются на апротонные и протолитические. Апро-тонные растворители не вступают в протолитическое взаимодействие с растворенным веществом. К ним относятся четыреххлори-стый углерод, толуол и др. Протолитические растворители участвуют в кислотно-основных процессах. Цо способности отщеплять и присоединять протоны протолитические растворители разделяют на отдельные группы. Растворители, легко присоединяющие протоны, называются протофильными, легко отщепляющие протоны - протогенными, способные присоединять и отщеплять протоны - амфипротонными. Та же классификация применяется и к другим веществам. [15]
Страницы: 1 2