Значение - константа - скорость
Cтраница 2
Значения констант скоростей каждой из элементарных стадий сохраняют постоянство только для одной температуры и потенциала, так как изменение этих параметров, влияя на величину активационного барьера реакции, изменяет и константу. При температурах выше 5 С выход по току и скорость синтеза НС1О4 резко падают из-за понижения на 6 порядков поверхностной концентрации хшосорбированного хлора и соответственно хлор-кислородных частиц. При понижении температуры ниже - 30 С происходит вытеснение активного окисла хемосорбированными перхлорат-радикалами. [16]
Значение константы скорости практически не зависит от концентрации ( до 0 3 моль / л) образующейся п-толуиловой кислоты. Лимитирующей стадией, по-видимому, является образование аддукта, а не его ионная перегруппировка в продукты, о чем свидетельствуют протекание реакции по закону второго порядка даже при избытке альдегида и слабая зависимость константы скорости от кислотности среды. [17]
Значения констант скорости ( к Ю3 мин. [18]
Значение константы скорости для движения иона k должно в некоторой степени отличаться от значения константы скорости для вязкого течения. Однако приближенно можно считать, что константа скорости k для диффузии ионов как в отсутствии, так и при наличии внешнего поля равна константе скорости вязкого течения растворителя, как было предположено на стр. [19]
Значения констант скоростей этой реакции определены при разных температурах сначала в отсутствие катализатора, а затем при добавлении иода. Энергия активации вычислялась с помощью уравнения Аррениуса и для каждого случая получено свое значение. Таким путем и обнаружено, что присутствие иода снижает энергию активации данной реакции. [20]
Значения констант скорости в массе и в растворе одинаковы. [21]
Значение константы скорости указывает на то, что возбужденная молекула сенсибилизатора ( А) в 100 раз быстрее вступает во взаимодействие с углеводом, чем в побочную реакцию с А, приводящую к распаду молекулы сенсибилизатора. [22]
Значения констант скорости для участков 1 - 2 и 3 - 4 приведены в таблице. [23]
Значения констант скорости одной из таких реакций в зависимости от добавок приведены ниже. [24]
Значение константы скорости К в зависимости от концентрации азотной кислоты и температуры приведены на рис. ПО. [25]
Значения константы скорости k в уравнении ( I), полученные Бон-никсеном, Чансом и Теореллом для чистой эритроцитной каталазы и каталазы из печени при 22, равны соответственно 3 5 107 и 3 0 10; Ж 1 сек-1. Энергия активизации в случае реакции эритроцитной каталазы имеет необыкновенно низкую величину, равную 1700 100 кал. [26]
Значения константы скорости выделены курсивом. Относительное сечение приведено в скобках, причем за единицу принято значение при минимальной энергии ионов. [27]
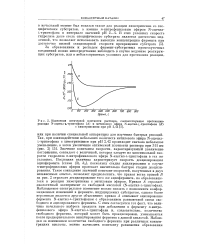 |
Изменение оптической плотности раствора, соответствующее протеканию реакции К-ацетил-ь - триптофана ( А и метилового эфира К-ацетил-ь - триптофана ( В. [28] |
Значение константы скорости, характеризующей увеличение поглощения, совпадает с величиной, которая следует из максимальной скорости гидролиза тг-нитрофенилового эфира М - ацетил-ь-триптофана в тех же условиях. Последняя величина характеризует скорость деацилирования ацилфермента [ схема ( 3), k3 ], поскольку стадия ацилирования в случае тг-нитрофениловых эфиров протекает значительно быстрее стадии деацилирования. Такое совпадение значений констант скоростей, полученных в двух независимых опытах, позволяет предположить, что правая ветвь кривой Б на рис. 2 отражает деацилирование того же ацилфермента, но образовавшегося в реакции химотрипсина с метиловым эфиром. Наблюдаемое спектральное изменение можно связать с появлением конфор-мационных изменений в ферменте, индуцируемых субстратом, однако более вероятным является другое объяснение: кривая А описывает ацилирование фермента N-ацетил-ь - триптофаном с образованием равновесной смеси свободного и ацилированного фермента. С этим согласуется тот факт, что величина начального выброса продукта при добавлении к ферменту тг-нитрофенилового эфира 1Ч - ацетил-ь-триптофана и, следовательно, количество свободного фермента, который может быть проацилирован, уменьшаются после предварительного инкубирования фермента с данной кислотой. [29]
 |
Зависимость нижнего предела давления самовоспламенения 2СО - J - О а от содержания этана в смеси при различных температурах. [30] |
Страницы: 1 2 3 4