Расчет - процесс - дистилляция
Cтраница 1
Расчет процессов дистилляции основывается на использовании уравнений материального и теплового балансов. [1]
Расчет процессов дистилляции основывается на использовании уравнений материального и теплового балансов и фазового равновесия. [2]
В расчетах процессов дистилляции отклонение системы от идеальной учитывается так называемым коэффициентом активности, характеризующим активность молекул в растворе и их взаимодействие. [3]
В расчетах процессов дистилляции отклонение системы от идеальной характеризуется величиной так называемого коэффициента активности, характеризующего активность молекул в растворе, их взаимодействие. [4]
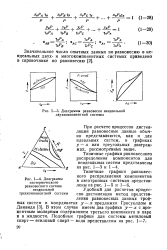 |
Диаграммы равновесия неидеальной двухкомпонентной системы. [5] |
При расчете процессов дистилляции равновесные данные обычно представляются, как и для идеальных систем, в графиках у - х или треугольных диаграммах, рассмотренных выше. [6]
 |
Диаграмма равновесия идеальной двухкомпонентной системы.| Диаграмма изотерм и-ческого р авновесного состава. [7] |
В расчетах процессов дистилляции отклонение системы от идеальной учитывается так называемым коэффициентом активности, характеризующим активность молекул в растворе и их взаимодействие. [8]
При расчете процессов дистилляции равновесные данные обычно представляются, как для идеальных систем, в графиках у - х или треугольных диаграммах. [9]
Значительный интерес для расчета процессов дистилляции представляет метод Ван-Лаара, предусматривающий изменение температуры и теоретически лучше обоснованный, чем метод Маргулеса. [10]
Следовательно, для расчета процесса дистилляции я-компонент-ной смеси имеется одно уравнение материального баланса ( 1.3 а), п - 1 уравнений (1.36) ил - 1 уравнений (1.2), которые в сочетании сп - 1 уравнениями равновесия дают возможность определить 2 / г - 1 неизвестных величин. Таким образом, для расчета процесса дистилляции - компонентной смеси необходимо решить систему 2п - 1 уравнений, из которых п уравнений алгебраические и п - 1 интегральные. Аналитическое решение такой задачи чрезвычайно затруднительно. Поэтому целесообразно выполнять расчет численными методами. [11]
Так, например, для расчета процессов дистилляции и ректификации пользуются диаграммами температура кипения - состав, по которым можно определить равновеаные составы жидкости и пара при любой температуре и проследить ход процессов испарения или конденсации. [12]
Диаграмма фазового равновесия смеси показана на рис. 137 Расчет процессов дистилляции, ректификации и конденсации смесей удобнее всего проводить, пользуясь графиками фазовых равновесий. По оси абсцисс графика откладывают состав смеси, по оси ординат - величины другого произвольно выбранного параметра. На оси ординат нанесены в верхней части рис. 137 температуры смеси, в нижней части рисунка - давление. Вертикальная линия, проведенная через точку / Сд, соответствует чистому компоненту А, вертикальная линия, проведенная через точку / Св. [13]
Знание коэффициентов разделения, получаемых из приведенных соотношений, позволяет применять обычные методы расчета процессов дистилляции, абсорбции, экстракции и других многостадийных процессов. [14]
Для определения плотностей жидкостей в широких диапазонах Т и Р рекомендуется метод Томсона, Бробс-та и Ханкинсона; в тех случаях, если требуется согласованность со свойствами пара, например при расчетах процессов дистилляции, вполне пригодно уравнение Пенга - Робинсона. [15]
Страницы: 1 2