Расчет - растворимость
Cтраница 2
Поэтому расчет растворимости по уравнению ( VIII, 36) приводит к расхождению с опытом: вопреки этому уравнению, растворимость, выраженная в мольной доле, зависит от природы растворителя. [16]
Поэтому расчет растворимости по ( VIII, 36) приводит к расхождению с опытом: вопреки этому уравнению растворимость, выраженная в мольной доле, зависит от природы растворителя. [17]
Рассмотрим расчет растворимости в воде компонентов газовой смеси, в которой нет какого-либо одного компонента с существенно преобладающей концентрацией. [18]
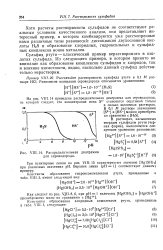 |
Распределительная диаграмма для сероводорода. [19] |
Хотя расчеты растворимости сульфидов не соответствуют реальным условиям качественного анализа, они представляют интересный пример, в котором комбинируются уже рассмотренные нами различные типы равновесий: диссоциация двухосновной кислоты H2S и образование хлоридных, гидроксильных и сульфидных комплексов ионов металлов. [20]
Осуществлен расчет растворимости гидроксидов железа ( III), хрома ( III), цинка ( II), кадмия ( II), кобальта ( II), никеля ( II), меди ( II), марганца ( II) и свинца ( II) в водных растворах, основанный на учете суммарных концентраций катиона металла и всех его гидроксокомплексов, рассчитываемых из произведений растворимости гидроксида металла, констант гидролиза, общих или ступенчатых констант образования комплексов и ионного произведения воды. Проведено сопоставление минимальной растворимости гидроксидов тяжелых металлов со значениями предельно-допустимых концентраций ( ПДК) ионов металлов в водоемах. Для водоемов культурно-бытового и хозяйственно-питьевого водопользования достижение значений ПДК возможно только для гидроксидов хрома, меди и марганца. [21]
 |
Значения коэффициентов k и т при 50 С в уравнении IV-38. [22] |
Для расчета растворимости предложен ряд эмпирических уравнений. [23]
Для расчета растворимости в граммах на 1 дм3 умножают молярную концентрацию на молекулярную массу вещества. Формула (3.31) справедлива в том случае, если можно пренебречь влиянием ионной силы раствора и протеканием конкурентных реакций. [24]
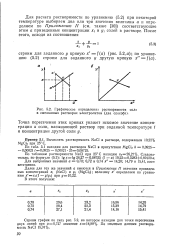 |
Графическое определение растворимости соли в смешанных растворах электролитов ( два способа. [25] |
Для расчета растворимости по уравнению (5.2) при некоторой температуре выбираем два или три значения величины а и определяем по Приложению II ( см. также [30]) соответствующие этим а приведенные концентрации х и г / i солей в растворе. [26]
Для расчета растворимости гелия по уравнению ( 102) значения Кр выбираются по графикам рис. 50 исходя из общего давления р и температуры Т смеси. Значения летучести чистого гелия, приведенные в табл. 34, были вычислены в работе [93] по уравнению Битти - Бриджмена. [27]
Для расчета растворимости газов в кристаллических полимерах следует делать поправку на кристалличность полимера. [28]
Для расчета растворимости малорастворимого газа, находящегося под большим давлением, служит уравнение И. Р. Кри-чевского - Я - С. [29]
Для расчета растворимости хлорида серебра в 0 1 F растворе азотной кислоты необходимо определить средний коэффициент активности хлорида серебра. Хотя в дейстаительности ионная сила раствора зависит от концентраций всех ионов, вклад растворимого хлорида серебра незначителен. [30]
Страницы: 1 2 3 4