Расчет - уровни - энергия
Cтраница 1
Расчеты уровней энергии по методу МОХ и отсюда общей энергии сопряженных систем не требуют a priori знания или расчета распределения зарядов и могут быть проведены без использования этого распределения зарядов. Ранние квантовомеханиче-ские расчеты карбониевых ионов в основном касались я-элек-тронной энергии сопряженных карбоний-ионов относительно незаряженных сопряженных молекул, из которых эти ионы могут быть получены. Эти разности энергий могут быть поэтому с некоторым приближением связаны с константами образования ионов карбония. На возможность расчета констант равновесия образования карбониевых ионов по этому методу было указано Уэлан-дом [1329, 1330], но из-за отсутствия подходящих экспериментальных данных он не был тогда существлен. Тем же методом была предсказана устойчивость ряда карбоний-ионов до того, как они были получены в действительности ( разд. [1]
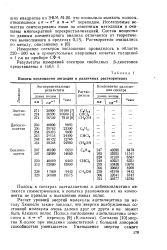 |
Полосы поглощения лигандов в различных растворителях. [2] |
Расчет уровней энергий молекулы ацетилацетона по методу Хюккеля также показал, что энергии возбужденных состояний молекулы очень далеки друг от друга и не может быть близких полос. Согласно [10] энергия К-полос при введении заместителей с большей донорной способностью уменьшается. [3]
При расчете уровней энергии л-электронов ( и распределения зарядов) методом МОХ принимается, что каждый л-электрон движется в кулоновском поле жесткой решетки расположенных на равном расстоянии и идентичных заряженных центров, соответствующих атомам углерода сопряженной системы, и в однородном поле других электронов. Ошибки, заложенные в этих постулатах, по-видимому, в значительной степени самопогашаются или же уменьшаются подходящим выбором величин р, поскольку расчет резонансных энергий сопряженных молекул методом МОХ, безусловно, дает очень хорошие результаты. [4]
При расчете уровней энергии изолированного атома или иона по схеме Рассела - Саундерса ( стр. В теории кристаллического поля поступают точно так же, учитывая, кроме того, на соответствующем этапе возмущающее действие кристаллического поля. [5]
При расчетах уровней энергии сложных атомов за основу берут уровни энергии атома водорода и с помощью теории возмущений приближенно определяют изменения этих уровней, вызванные влиянием других электронов. Но для проведения таких расчетов требуется дальнейшая схематизация атома, правомерность которой обоснована в настоящее время квантовой механикой. Мы рассмотрим сначала системы, о которых известно ( например, из химических свойств соответствующих элементов), что они состоят из отдельного, так называемого валентного электрона, слабо связанного с атомным остатком, образованным из Z-кратно заряженного ядра и Z - 1 электрона. Такого рода системами являются атомы щелочных элементов, а также Си, Ag, Аи. Эффективный заряд, в поле которого находится валентный электрон, оказывается равным единице благодаря экранирующему действию электронов атомного остатка. Если полностью пренебречь возмущением, создаваемым этими электронами, мы получим систему водородных термов. Уже давно известно, что спектры щелочных металлов обнаруживают значительное сходство со спектром водорода. [6]
Описанная схема расчета уровней энергии многоэлектронного атома применима при условии, что взаимодействия можно расположить в последовательности: действие на электроны эффективного потенциала ( одночастичное приближение), остаточное взаимодействие, спин-орбитальное взаимодействие. У большинства атомов величина магнитного взаимодействия спин - спин и спин - орбита имеет один и тот же порядок и меньше остаточных. В таком случае рассмотренная схема применима и говорят об L - S-связи, для которой характерно сложение при расчете отдельно орбитальных и отдельно спиновых моментов. Исключения представляют некоторые тяжелые атомы с почти полностью заполненными оболочками: у них взаимодействия спин - спин много больше взаимодействий орбита - спин и больше остаточных. В таком случае правомерен другой порядок сложения моментов импульса и другой метод определения терма. Кроме того, нередки случаи, когда спин-орбитальные и остаточные взаимодействия близки по величине. [7]
Рассмотренный способ расчета уровней энергии стационарных состояний дает хорошие результаты для простых атомов начала периодической системы элементов. [8]
Качественный анализ и расчет уровней энергии, произведенный выше, справедливы только для достаточно слабых полей. [9]
Более точные методы были применены также для расчета уровней энергии гелия и небольшого числа других простых молекул, кроме водорода. Однако эти расчеты даже и в случае водорода и гелия являются чрезвычайно сложными. [10]
Обобщенный метод Хюккеля был применен в работе [65] для расчета уровней энергии, прочности связи и заряда на атоме металла хемосорбционных комплексов окиси углерода и окиси азота с переходными металлами четвертого периода. [11]
Для 5 3 / 2 или для произвольного направления внешнего поля расчет уровней энергии делается громоздким и не приводит к простым формулам. [12]
По-видимому, наиболее важно применение теории возмущений в теории валентности для расчета уровней энергии комплексов переходных металлов. [13]
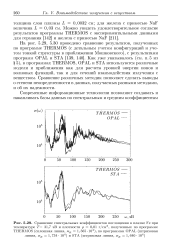 |
Сравнение спектральных коэффициентов поглощения в плазме Fe при. [14] |
THERMOS, OPAL и STA используются различные модели и приближения как для расчета уровней энергии ионов и волновых функций, так и для сечений взаимодействия излучения с веществом. Сравнение различных методик позволяет сделать выводы о степени неопределенности в данных, получаемых разными методами, и об их надежности. [15]
Страницы: 1 2