Расчет - энергия
Cтраница 4
Относительно расчета энергии, образования газообразных комплексных ионов по Яцимирскому см. соответствующую оригинальную литературу. [46]
Для расчета энергии, переносимой электромагнитным полем, необходимо дополнительно знать распределение энергии в поле, что будет рассмотрено в следующей главе. [47]
Для расчета энергии гидратации строят так называемый цикл Борна - Габе-ра, в котором отражены различные пути проведения этого перехода. [48]
Для расчета энергии Гиббса и констант равновесия при температурах выше температур фазовых переходов реагирующих веществ предложено несколько методов. [49]
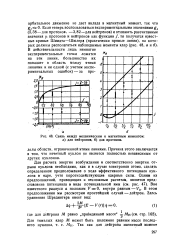 |
Связь между механическим и магнитным моментом. а для нейтронов, б для протонов. [50] |
Для расчета энергии возбуждения и соответственно энергии, отрыва нуклрна необходимо, как и в случае электронов атома, сделать определенное предположение о ходе эффективного потенциала нуклона в ядре, учтя короткодействующие ядерные силы. В этом предположении мы рассмотрим простейший случай-дейтрон. [51]
 |
Зависимость энергии взаимодействия от расстояния для тел различной формы. [52] |
Для расчета энергии адсорбции, кинетики газов в порах и капиллярах важно знать потенциалы взаимодействия атомов и молекул с поверхностями различной геометрической формы. [53]
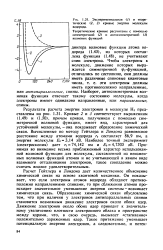 |
Экспериментальная ( / и теоретические ( 2, 3 кривые энергии молекулы водорода. [54] |
Результаты расчета энергии электронов в молекуле Н2 представлены на рис. 1.31. Кривые 2 и 3 соответствуют выражениям (1.49) и (1.50), причем кривая, полученная с помощью симметричной волновой функции, имеет вид, характерный для устойчивой молекулы, - она показывает образование химической связи. [55]
 |
Экспериментальная ( / и теоретические ( 2, 3 кривые энергии молекулы водорода. [56] |
Результаты расчета энергии электронов в молекуле Н2 представлены на рис. 1.31. Кривые 2 к 3 соответствуют выражениям (1.49) и (1.50), причем кривая, полученная с помощью симметричной волновой функции, имеет вид, характерный для устойчивой молекулы, - она показывает образование химической связи. [57]
Страницы: 1 2 3 4