Точный термодинамический расчет
Cтраница 1
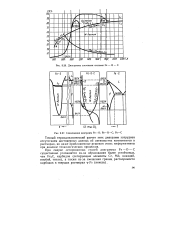 |
Диаграмма состояния системы Fe - О - С.| Совмещение диаграмм Fe-О. Fe-О - С. Fe-С. [1] |
Точный термодинамический расчет этих диаграмм затруднен отсутствием достоверных данных об активностях компонентов в растворах, но даже приближенные решения очень информативны при анализе технологических процессов. [2]
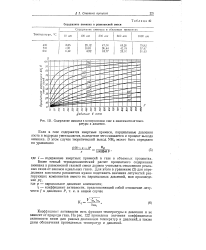 |
Содержание аммиака в конверсионном газе в зависимости от температуры и давления. [3] |
Более точный термодинамический расчет процентного содержания аммиака в равновесной газовой смеси должен учитывать отклонения реальных газов от законов идеальных газов. [4]
Для точного термодинамического расчета систем, содержащих большие количества щелочных металлов и кислорода, при температурах более низких, чем приведенные выше, необходимо учитывать образование твердых окислов. [5]
В настоящее время описанный способ является наиболее употребительным при точных термодинамических расчетах. [6]
Это расхождение, рчевидно, объясняется весьма приближенным значением термодинамических функций, принятых для расчета реакции гидрохлорирования пропилена, и еще раз подтверждает необходимость проведения более точных термодинамических расчетов реакций гидрохлорирования непредельных углеводородов. [7]
Однако в тех случаях, когда мы имеем дело с особо точными, прецизионными экспериментальными данными ( такими, например, как наиболее точные даннне по удельным объемам водяного пара, находящегося в равновесии с кипящей водой) и в особенности с точными термодинамическими расчетами, где фигурируют производные различных величин по температуре, пренебрежение разницей между Т и 7 е д в расчетах по термодинамическим уравнениям может привести к погрешностям, соизмеримым с погрешностью собственно экспериментальных данных. [8]
Данные химической термодинамики позволяют нам предварительно оценить максимально возможные выходы спирта в определенных условиях. Наиболее подробные и точные термодинамические расчеты по реакции присоединения воды к этилену опубликованы А. А. Введенским и Я. [9]
 |
Зависимость удельного удерживаемого объема на 1 г насадки от процента пропитки хромосорба W Р Р - дицианди-этилсульфидом, иллюстрирующая влияние адсорбции на поверхности жидкости. [10] |
Статические измерения, проведенные Пексоком и Гампом [18], показали, что адсорбция полярных веществ наблюдается и на поверхности неполярных жидкостей. Это требует введения соответствующих поправок при точных термодинамических расчетах. [11]
Кроме того, закон Дюлонга и Пти не учитывает температурную зависимость теплоемкости твердых тел. Правда, для большинства твердых тел при средних и высоких температурах температурная зависимость теплоемкости весьма слаба, однако в точных термодинамических расчетах ее необходимо учитывать. Отсюда следует, что закон Дюлонга и Пти может быть применен лишь при не очень точных расчетах. [12]
Однако отклонения газообразных компонентов от законов идеального газового состояния ограничивают применение вышеприведенного уравнения. Точный термодинамический расчет равновесия при более высоких давлениях необходимо отложить до накопления экспериментальных данных по свойствам газообразных компонентов реакции при более высоких давлениях и отсюда - вывода для них соответствующих уравнений состояния. [13]
Эти опыты, безусловно, говорят о том, что при синтезе бутадиена из спирта дегидратация не может предшествовать конденсации. Происходит ли эта задержка на основании термодинамических или же кинетических причин, можно решить на основани точного термодинамического расчета равновесия. [14]
Левая часть уравнений (6.2) и (6.3) выражает абсолютную энтальпию ( внутреннюю энергию) исходной горючей смеси при начальной температуре Т0, а правая - энтальпию ( внутреннюю энергию) смеси продуктов горения при температуре горения 7Y или взрыва Гвзр. Детальная методика расчета температуры горения органических соединений, основанная на этих представлениях, описана в следующих двух разделах. При этом рассматриваются только системы, образованные углеродом, водородом, кислородом, азотом и аргоном, так как точный термодинамический расчет систем, содержащих другие элементы, без применения ЭВМ чрезвычайно сложен и выходит за рамки предлагаемой книги. Приближенные методы расчета малоэффективны, поэтому тоже не приводятся. [15]
Страницы: 1 2