Расщепление - электронные уровни
Cтраница 2
Система электронных уровней в жидкостях должна зависеть от среднего расстояния между атомами, которое меняется в широких пределах. Электрические поля, обусловленные соседними атомами, и расщепление электронных уровней отдельных атомов, вызванное этими полями, отчасти отличаются для разных атомов. Поэтому вырождение может сниматься, и часто более правильно рассматривать электроны связанными с отдельными атомами. Тепловое движение приводит к тому, что часть внешних электронов атомной оболочки переходит в свободное состояние. [16]
Для простых тетраэдрических кристаллов с ковалентной связью строятся связывающие орбитали из 5р3 - гибридизованных орбиталей. Энергия связывающих орбиталей выражается через энергию ковалентной связи V % и энергию-ионной связи V3, Расщепление электронных уровней атомов в зоны описывается матричными элементами между различными связывающими состояниями. Для предварительного анализа зонной структуры идеальных кристаллов энергии всех зон при k0 выражаются через матричные элементы из ОПСЭ, При расчете других характеристик использование метода связывающих орбиталей устраняет необходимость искать сами энергетические зоны и позволяет описать характер химической связи в идеальных кристаллах и аморфных твердых телах. Ошибки, возникающие при использовании метода связывающих орбиталей, можно учесть, если построить расширенные связывающие орбитали с помощью теории возмущений. Обе основные характеристики ковалентной связи, степень ионности и степень металличности, определяются через параметры из ОПСЭ. [17]
Отдельные разрозненные атомы металлов в состоянии пара не обладают электропроводностью, но отличаются малыми значениями ионизационных потенциалов. При уменьшении температуры и конденсации паров металла в жидкий, а затем и твердый проводник, происходит расщепление энергетических электронных уровней атомов вследствие сил электрического взаимодействия. Каждый уровень энергии атома, заполненный электронами, или тот, в котором электроны могут находиться в возбужденном состоянии, распадается на ряд уровней, число которых равно числу атомов, образующих проводник. В металлах, как это видно из фиг. [18]
Введение в комплекс типа МА6 иных аддендов, например аддендов В с образованием комплекса МА4В2, приводит к искажению октаэдра, понижению его симметрии, а следовательно, к расщеплению электронных уровней. При этом увеличивается число полос поглощения. Действительно, часто менее симметричные мс-изомеры отличаются более сложным спектром поглощения. Иногда полосы поглощения в спектре ыс-изомера смещены относительно полос поглощения транс-формы ( табл. 83), Однако некоторые изомеры отличаются лишь интенсивностью полос поглощения, но не их положением. [19]
Происходит расщепление как электронных уровней атомов и молекул, так и вращательных уровней молекул, обладающих дипольным электрическим моментом. Величина расщепления электронных уровней энергии в сильных полях ( порядка десятков и сотен тысяч вольт па сантиметр) достигает десятитысячных и тысячных долей электрон-вольта. Для вращательных уровней энергии в применяемых электрических полях порядка тысяч вольт на сантиметр величина расщепления составляет миллионные доли электрон-вольта. В видимой и ультрафиолетовой областях спектра наблюдается расщепление спектральных линий атомов в электрическом поле, соответствующее расщеплению электронных уровней энергии, которое носит название эффекта Штарка. Расщепление вращательных уровней дипольных молекул в электрическом поле может изучаться непосредственно радиоспектроскопическим методом электрического резонанса. [20]
В настоящее время необходимо предъявлять повышенные требования ко всем исследованиям адсорбции спектральными методами. В связи с этим особенно важен выбор систем для исследования и спектральных параметров взаимодействия, которые наиболее полно характеризовали бы механизм адсорбции. Получаемая этими методами информация о расщеплении электронных уровней указывает на тип симметрии окружающего катион силового поля, перераспределение электронной плотности и тем самым характеризует место фиксации катиона в решетке цеолита и расположение адсорбированных молекул по отношению к катиону. Этот случай интересен также тем, что для интерпретации результатов может быть применена теория поля лигандов - интенсивно разрабатываемая в настоящее время область квантовой химии. [21]
Вторая теорема, теорема Крамерса, утверждает, что чисто электростатическое поле, которое действует на систему с нечетным числом электронов, всегда оставляет ее уровни двукратно вырожденными. И действительно, между двумя уровнями такого дублета в присутствии магнитного поля может наблюдаться магнитный резонанс. Если бы теорема Крамерса не имела места, то расщепления электронных уровней в ионе были бы слишком большими и мы не могли бы исследовать переходы, соответствующие парамагнитному резонансу на той полосе частот, которую нам предоставляют генераторы СВЧ. [22]
Электроны парамагнитных ионов находятся обычно в сильных электрических полях кристаллической решетки или сольватной оболочки в случае растворов. Электрические поля полностью или частично снимают орбитальное вырождение и через спин-орбитальную связь изменяют расщепление электронных уровней. [23]
Ряд работ был посвящен теории оптической активности спиральной цепи. Основываясь на теории А. С. Давыдова, согласно которой подобное взаимодействие в системе, обладающей дальним порядком, приводит к экситонному расщеплению электронных уровней [ ] ( см. стр. [24]
К первой группе можно отнести полимеры, к которым при-ложимы представления, развитые для молекулярных кристаллов. К ним относятся полимеры с линейной системой сопряженных связей. Можно показать [13], что рост полимерной цепи не сопровождается увеличением сопряженной системы и участки сопряжения имеют примерно одинаковые строение и длину в различных образцах, независимо от молекулярного веса. При этом, несмотря на расщепление электронных уровней отдельных структурных единиц, составляющих полимерную молекулу, они не образуют квазинепрерывную зону, охватывающую всю молекулу, и расстояния между соседними уровнями остаются большими ввиду ограниченной длины участков непрерывного сопряжения. Между молекулами действуют дисперсионные силы, и если зоны, охватывающие полимерные молекулы, и образуются, то очень узкие, и их ширина не превышает kT ( см. гл. Обычно эти полимеры по проводимости близки изоляторам. К этой же группе относятся полимеры, образующие донорно-акцепторные комплексы с молекулами введенных акцепторов или внутримолекулярные комплексы. [25]
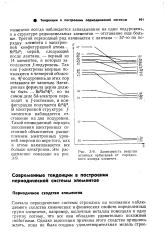 |
Зависимость энергии атомных орбиталей от порядкового номера элемента. [26] |
Третий переходный ряд начинается с лантана - 57-го по порядку элемента с электронной конфигурацией атома... Так как / - электроны впервые появляются в четвертой оболочке, 4 / - подуровень до этих пор оставался не занятым. В электронной структуре / - элементов наблюдается отставание на два подуровня. Такой неожиданный порядок заполнения электронных состояний объясняется расщеплением электронных уровней энергии по мере того, как в атоме накапливается все больше электронов. [27]
Третий переходный ряд начинается с лантана - 57-го по порядку элемента с электрон - ной конфигурацией атома... Так как / - электроны впервые появляются в четвертой оболочке, 4 / - подуровеньдоэтих пор оставался не занятым. В электронной структуре / - элементов наблюдается отставание на два подуровня. Такой неожиданный порядок заполнения электронных состояний объясняется расщеплением электронных уровней энергии по мере того, как в атоме накапливается все больше электронов. [28]
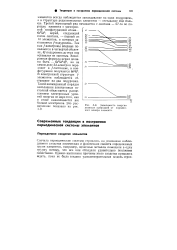 |
Зависимость энергии атомных орбиталей от порядкового номера элемента. [29] |
Третий переходный ряд начинается с лантана - 57-го по порядку элемента с электронной конфигурацией атома... Gs Sd1; церий, следующий после лантана, - первый из 14 элементов, в которых заполняется / - подуровень. Так как / - электроны впервые появляются в четвертой оболочке, 4 / - подуровень до этих пор оставался не занятым. В электронной структуре / - элементов наблюдается отставание на два подуровня. Такой неожиданный порядок заполнения электронных состояний объясняется расщеплением электронных уровней энергии по мере того, как в атоме накапливается все больше электронов. [30]
Страницы: 1 2 3