Реакция - диссоциация
Cтраница 2
Реакции диссоциации комплексов обычно имеют первый или псевдо-первый порядок [ 1, стр. [16]
Реакции диссоциации трехатомных молекул можно разделить на две группы в зависимости от того, разрешены или запрещены они в соответствии с правилом сохранения спинового момента. К первой группе относятся реакции без изменения электронного состояния, происходящие на потенциальной поверхности основного синглетного состояния диссоциирующей молекулы. Как и в случае реакции двухатомных молекул, при [ М ] 10 - 4 моль / см3 диссоциация и рекомбинация молекул этой группы почти всегда протекает в области низкого давления. [17]
Реакция диссоциации пятихлорного фосфора протекает по уравнению PCls1 РСЗя СЬ. [18]
 |
Зависимость степени диссоциации N204 от температуры. [19] |
Реакция диссоциации четырехокиси азота N2O4 при повышении температуры или понижении давления, как и обратная реакция димеризации окиси азота NO2 при понижении температуры или повышении давления, является классическим примером обратимой химической реакции, равновесие которой в сильной степени зависит от температуры и давления. [20]
Реакция диссоциации водяного пара, обратная процессу горе-ия водорода, может протекать в той или иной мере в горячем пламени водорода, реагирующего с кислородом. [21]
Реакция диссоциации окиси углерода с выделением свободного атомарного углерода обычно протекает на поверхности стали, которая оказывает на нее каталитическое действие. При температуре нагрева выше точки Ас, в стали происходит фазовое превращение Fea в Ре7, чем обеспечивается возможность растворения образовавшегося атомарного углерода в FeT. [22]
Реакции диссоциации комплекса Cd ( CN) 3 отвечает константа скорости & - 8 0 - 105 сек 1 при ионной силе 0 1 - Образование комплексов Cd ( CN) r из Cd ( CN) 2 - происходит обратимо. [23]
Реакция диссоциации окиси углерода с выделением атомарного углерода обычно протекает на поверхности стали, которая оказывает на нее каталитическое действие. [24]
Реакция диссоциации слабых электролитов описывается законом действующих масс и характеризуется константой и степенью диссоциации. [25]
Если реакция диссоциации не включает стадию разделения зарядов, сила кислот или оснований мало зависит от диэлектрической проницаемости растворителя. [26]
При реакции диссоциации правая часть уравнения реакции имеет один член С - диссоциирующееся вещество. [27]
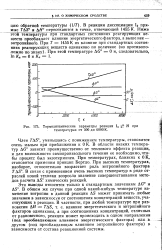 |
Термодинамические параметры реакции 12 21 при температурах от 300 до 6000 К. [28] |
В реакции диссоциации 12 прямые T & S я A / f пересекаются в точке, отвечающей 1455 К. Ниже этой температуры При стандартных состояниях реагирующих ве - - ществ преобладает влияние энергетического фактора, а выше нее - энтропийного. [29]
Это реакция диссоциации ( распада целого на части) галита на свободные ионы с образованием раствора электролита. [30]
Страницы: 1 2 3 4