Реакция - термическая диссоциация
Cтраница 1
Реакции термической диссоциации окислов и карбонатов хорошо изучены. Они играют важную роль в металлургических процессах. Для практики представляет большой интерес температура, при которой упругость диссоциации карбоната ( или окисла) становится равной величине внешнего ( нормального) атмосферного давления. Ее иногда называют температурой разложения. Ниже этой температуры под атмосферным давлением разложение указанных веществ почти е наблюдается. [1]
Реакция термической диссоциации полуторных окислов РЗЭ до моноокислов лишь для La2O3 может давать заметный вклад в общий поток компонентов, поступающих в газовую фазу при температурах в кратере электрода 2000 К. Поданным термодинамического анализа реакция термической диссоциации окислов РЗЭ до металлов, а также реакция восстановления до моноокислов углеродом существенно не влияет на скорость поступления РЗЭ в газовую фазу. [2]
Реакции термической диссоциации окислов и карбонатов хорошо изучены. Они играют важную роль в металлургических процессах. Для практики представляет большой интерес температура, при которой упругость диссоциации карбоната ( или окисла) становится равной величине внешнего ( нормального) атмосферного давления. Ее иногда называют температурой разложения. Ниже этой температуры под атмосферным давлением разложение указанных веществ почти не наблюдается. [3]
Все реакции термической диссоциации эндотермичны и требуют затрат тепла на их осуществление. [4]
Начало реакции термической диссоциации связано с возникновением центров реакции, зародышей новой фазы. [5]
Следовательно, реакция термической диссоциации NH4CI является эндотермической. Поэтому тепловой эффект реакции образования соединений из простых веществ равен стандартной теплоте их образования. [6]
 |
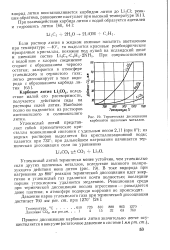
Ступенчатая дегидратация CuSO4 5Н2О в вакууме при 50вС. [7] |
Равновесие в реакциях термической диссоциации кристаллогидратов, как и в реакции ( а), характеризуется давлением диссоциации Рнго, которое для данной температуры является величиной постоянной и не зависит от количеств безводной и гидратированной соли. [8]
Вследствие большей прочности НП4 константа реакции термической диссоциации его должна быть меньше соответствующей константы для ZrI4, поэтому одинаковая степень диссоциации в случае гафния достигается при более высокой температуре нити. [9]
Проведено термодинамическое исследование возможности протекания реакций термической диссоциации, реакций восстановления углеродом и реакций образования и диссоциации дикарбидов РЗЭ. [10]
При 30 С константа равновесия реакции термической диссоциации SOzCIjfr) ч SOj ( r) С12 ( Г) равна 2 9 - Ю-2. [11]
Более высокие температуры способствуют протеканию реакций термической диссоциации урано-ванадатов и ванадатов натрия, а также реакций взаимодействия их с двуокисью кремния. Образующиеся силикаты урана нерастворимы в карбонатных растворах и труднорастворимы в кислых растворах. При низких температурах соединения урана и ванадия не могут полностью перейти в растворимое состояние. [12]
Более высокие температуры способствуют протеканию реакций термической диссоциации урано-ванадатов и ванадатов натрия, а также реакций взаимодействия их с двуокисью кремния. Образующиеся силикаты урана нерастворимы в карбонатных растворах и труднорастворимы в кислых растворах. При низких температурах соединения урана и ванадия не мсгут полностью перейти в растворимое состояние. [13]
Ядерные реакции диссоциации ( как и реакции термической диссоциации молекул) вызываются кинетической энергией сталкивающихся частиц. [14]
 |
Термическая диссоциация карбонатов щелочных металлов. [15] |
Страницы: 1 2 3 4