Реакция - иод
Cтраница 2
Из уравнения реакции иода с тиосульфатом натрия окислительно-восстановительный эквивалент Na2S2O3 равен молекулярной массе. Кристаллический тиосульфат натрия имеет формулу Na2S2O3 - 5H20, однако состав его не бывает строго постоянным. [16]
Предполагается, что реакция иода с радикалами протекает очень быстро, и поэтому любые другие продукты помимо иодидов могут образоваться только за счет одновременно проходящей молекулярной реакции. Поэтому отношение иодидов к углеводородам в продуктах реакции дает возможность определить относительную важность двух типов механизма термического разложения. Метод, однако, представляет затруднение в отношении интерпретации результатов, ввиду их неоднозначности. [17]
По количеству вошедшего в реакцию иода вычисляют концентрацию сернистой кислоты и соответственно сернистого ангидрида. [18]
Методом непрерывной струи были исследованы реакции иода в растворах сульфита, содержащих ионы иода и кислоту. [19]
Катаев и Гостева [45] исследовали реакцию иода с цианидом серебра в смесях изобутилового спирта и четыреххлористого углерода при различных температурах. Оказалось, что скорость реакции зависит от вязкости среды. Близость энергии активации к теплоте диффузии указывает на то, что реакция лимитируется диффузией. В табл. 5.5 приведено сравнение теплот диффузии и энергий активации. [20]
В некоторых вариантах метода используют реакцию иода с гидразином. [21]
Применяется для титрования не вошедшего в реакцию иода. Раствор не может сохраняться в течение долгого времени, поэтому его готовят в небольшом количестве. Для повышения устойчивости раствора прибавляют 0 1 г карбоната натрия или 1 % ( по объему) амилового спирта и хранят раствор в хорошо закрывающейся склянке. [22]
Воду определяют титрованием не вошедшего в реакцию иода. [23]
Применяется для титрования не вошедшего в реакцию иода. Раствор не может сохраняться в течение долгого времени, поэтому его готовят в небольшом количестве. Для повышения устойчивости раствора прибавляют 0 1 г карбоната натрия или 1 % ( по объему) амилового спирта и хранят раствор в хорошо закрывающейся склянке. [24]
Воду определяют титрованием не вошедшего в реакцию иода. [25]
Вероятно, последний может образоваться и при реакции иода с радикалами алкокси-целлюлозы, полученными при гемолитическом разрыве глюко-зидных связей ( что отмечено также и другими исследователями [97]), а также связей элементарного звена. [26]
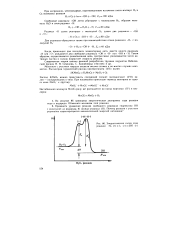 |
Энергетическая схема хода реакции Н2 ( г Ь ( г 2Н1 ( г. [27] |
На рисунке 86 приведена энергетическая диаграмма хода реакции иода и водорода. [28]
Трехиодистый висмут, BiI3, образуется непосредственно по реакции иода с висмутом ( 240 - 250) в атмосфере С02 или водорода. Его получают и действием иода на нагретый сульфид трехвалентного висмута или на смесь Bi203 с серой, взаимодействием йодистого этила С2Н51 с треххлористым висмутом и обработкой растворов солей висмута стехиометрическим количеством йодистого калия или натрия. [29]
Штромейером ( 1776 - 1835) была описана реакция иода с крахмалом, в результате которой развивается синяя окраска. И в настоящее время свежеприготовленный раствор крахмала широко используется в качестве специфического органического реагента на свободный иод. [30]
Страницы: 1 2 3 4