Реакция - ацилирование - анилин
Cтраница 1
Реакция ацилирования анилина протекает с низкими значениями энергии активации и энтропии активации. [1]
Реакции ацилирования анилина дихлорангидридами м - и га-кар-борандикарбоновых кислот характеризуются низкими значениями энергии активации и энтропии активации. [2]
 |
Влияние растворителя на энергию активации. а и предэкспоненииальный множитель А в реакции разложения N2O5. [3] |
Исследование кинетики реакции ацилирования анилина хлористым бензоилом показало, что при переходе от одного растворителя к другому резко изменяются константа скорости и энергия активации. Предэкспоненциальный множитель в уравнении Аррениуса остается практически неизменным. Однако для гетерополярных реакций можно ожидать при смене растворителя существенного изменения 2Даг, за счет чего значения А могут меняться на несколько порядков. Уравнения (218.19) и (218.20) справедливы и для реакций в газовой фазе. [4]
Исследование кинетики реакции ацилирования анилина хлористым бензонлом показало, что при переходе от одного растворителя к другому резко изменяются константа скорости и энергия активации. Предэкепоненциальпый множитель в уравнении Аррениуса остается практически неизменным. Однако для гетерополярных реакций можно ожидать при смене растворителя существенного изменения ЕАа, за счет чего значения А могут меняться на несколько порядков. Уравнения (218.19) и (218.20) справедливы и для реакций в газовой фазе. [5]
Изучена кинетика реакции ацилирования анилина, / г-нитроанилина, 4-аминобифенила, 4-амино - 4 -нитробифепила и 4-амино - 4 -нитро - 2 2 -димо-тилбифенила бензоилч лоридом, n - нитробензоилхлоридом и ацстплхлоридом и бензольном растворе. [6]
Изучена кинетика реакции ацилирования анилина монохлорангидридом лг-карборанкарбоновой кислоты в метиленхлориде, 1 2-дихлор-этане, трихлорэтилене и тетрахлорэтилене при трех температурах. [7]
Изучено влияние температуры, мольного отношения исходных компонентов и растворителей на реакцию ацилирования анилина 4 - НБК - Показана возможность синтеза 4 - НБА с выходом 88 % сплавлением анилина и 4 - НБК. [8]
Как видно из табл. 1 и 2, природа среды оказывает значительное влияние на величины Ki и Kz - Резкое увеличение скорости реакций ацилирования анилина в последних пяти растворителях табл. 1 и 2 можно объяснить специфической сольватацией молекул реагирующих веществ молекулами растворителей. [9]
Влияние неорганических солей при синтезе полимеров в амид-но-солевых растворителях двояко. Так, в работе [21] показано, что реакция ацилирования анилина изофталилхлоридом ускоряется солями металлов: в присутствии LiCl ( 1 77 моль / л) константа скорости возрастает примерно в 560 раз. [10]
Подробное изучение реакционной способности этих групп при нахождении их в одной молекуле до середины 1990 - х г. не проводилось. Однако, исходя из реакционной способности суль-фонилхлоридных и хлорангидридных групп, находящихся в разных молекулах, не представляет труда сделать вывод о том, что хлорангидридная группа обладает большей реакционной способностью, чем сульфонилхлоридная. Сравнение реакционной способности хлорформильных групп 18 в дихлорангид-риде терефталевой кислоты в реакции ацилирования анилина показало, что аминолиз протекает последовательно по каждой группе, причем, константы скоростей по 1 - й и 2 - й хлорангид-ридным группам составляют в условиях эксперимента 0.848 и 0.311 л-моль - с 1, соответственно. [11]
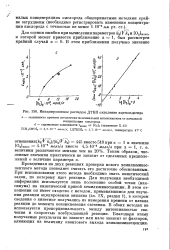 |
Инициированное распадом ДТБП окисление ацетальдегида. [12] |
Проведенная на двух реакциях проверка нового хемилюминес-центного метода позволяет считать его достаточно обоснованным. При использовании этого метода необходимо знать кинетический закон, по которому идет реакция. Для получения необходимой информации используется лишь положение особой точки ( максимума) на кинетической кривой хемилюминесценции. В этом отношении он имеет сходство с методом, применявшимся для изучения реакции ацилирования анилина ( гл. [13]
Страницы: 1