Реакция - метан
Cтраница 2
При проведении реакции метана с водяным паром при высокой температуре с целью получения водорода и окиси углерода наилучшим повидимому является никелевый катализатор, нанесенный на инертный огнеупорный материал. Данные, касающиеся срока службы таких катализаторов, несколько противоречивы, но присутствие соединений серы в газах повидимому вызывает уменьшение активности. При некоторых условиях, как утверждают Neumann и Jacob33, на катализаторе может происходить отложение свободного угля, особенно в тех случаях, когда газы содержат заметное количество - гомологов метана. Отложение свободного угля вызывает быстрое ухудшение катализатора и заставляет производить последующее оживление. Для уменьшения этого действия кажется благоприятным введение избытка пара. Однако - же Hawk, Golden, Storch и Fieldner и заметили, что увеличение концентрации водяного пара в реагирующих газах вызывает образование большого количества двуокиси углерода за счет окиси углерода без увеличения доли превращенного метана. [16]
 |
Схема работы эндотермического генератора для приготовления контролируемой атмосферы ( ЗИЛ и НИИТАвтопром. [17] |
Для ускорения реакции метана с кислородом электропечь наполняется катализатором ГИАП-3. При температуре 950 С кислород воздуха и метан вступают в реакцию. Получаемая атмосфера проходит через водяную рубашку 13 и попадает в хо - - лодильник 14 предварительного, охлаждения, где и охлаждаются до 300 С. После этого газ проходит в другой холодильник 15 и охлаждается в нем до комнатной температуры. Охлажденная атмосфера, состоящая из 20 % окиси углерода, 40 % водорода и 40 % азота, поступает в общий коллектор 16 и далее по трубам 17 направляется к термическим печам. В трубопроводе газовая смесь пропускается через фильтр 18 в прибор 19 с самописцем 20 для определения точки росы. Точкой росы называют температуру, при которой газ определенного состава, охлаждаясь при постоянном влагосодержании, становится насыщенным. [18]
В промышленности реакцию метана с водяным паром используют для получения водорода и смесей окиси углерода с водородом. [19]
Измеряя количество выделившегося при реакции метана, можно определить число подвижных атомов водорода в реагирующем веществе. Этот метод определения числа гидроксиль-ных, амидных, имидных и тому подобных групп в органических соединениях, предложенный Л. А. Чугаевым ( 1905) и разработанный его учеником Ф. В. Церевитиновым, пользуется всеобщим признанием и оказал бесчисленные услуги при выяснении строения различных веществ ( см. стр. [20]
Измеряя количество выделившегося при реакции метана, можно определить число подвижных атомов водорода в реагирующем веществе. [21]
 |
Схема лабораторной установки. [22] |
В образовании сероуглерода при реакции метана с серой принимают участие ненасыщенные углеводороды, главным образом этилен. [23]
Аналогично исследовалась температурная зависимость реакции метана. При температуре 300 С водород и окись углерода реагируют целиком. В условиях, когда ранее рассмотренные реакции уже полностью завершились, реакция с метаном только начинает проходить в заметной мере. [24]
Полученное уравнение удовлетворительно описывает скорость реакции метана с водяным паром. [25]
Есть и другие различия между реакциями метана и высших углеводородов, которые иллюстрируются приводимой ниже рабочей схемой окисления пропана СН3 СН2 СН3, не являющейся, впрочем, точно установленной во всех ее деталях. [26]
При этом тепло, необходимое для реакции метана с водяным паром, получалось за счет сгорания внутри реактора некоторого количества метана. Уже почти 30 лет рассматривается вопрос об использовании частичного внутреннего сожжения углеводородов для достижения высоких температур, которые требуются для получения ацетилена. [27]
Силилкарбанионы могут быть также получены при реакции полисилилировашюго метана с алкоксидом. Предполагают, что движущей силой этой реакции является термодинамически выгодное образование связи Si - О. [28]
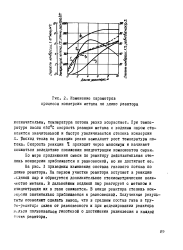 |
Изменение параметров процесса конверсии метана по длине реактора. [29] |
При температуре около 650 С скорость реакции метана с водяным паром становится значительной и быстро увеличивается степень конверсии X. Расход тепла на реакции резко замедляет рост температуры потока. Скорость реакции 1 проходит через максимум и начинает снижаться вследствие понижения концентрации компонентов сырья. [30]
Страницы: 1 2 3 4