Значение - перенапряжение
Cтраница 2
Ниже даны значения перенапряжения ( в мВ) выделения водорода из 16 % - ного раствора щелочи при 80 С на материалах, обычно применяемых для изготовления катодов, а также на платине. [16]
В табл. 2.1 представлены значения перенапряжения выделения Н2 и О2 при электролизе щелочных растворов в условиях, близких к условиям промышленной эксплуатации. [17]
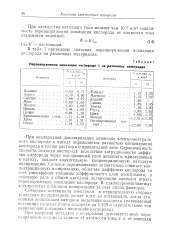 |
Перенапряжение ионизации кислорода 0 на различных электродах. [18] |
В табл. 7 приведены значения перенапряжения ионизации кислорода на различных материалах. [19]
В таблице дано сравнение значений перенапряжения для этих растворов с значениями перенапряжения для других щелочей. Как следует из рис. 1, потенциалы при соответствующих плотностях тока для растворов ( CH3) 4NOH и ( CH3) 4NJ - совершенно совпадают. Это совпадение представляет особый интерес и свидетельствует о том, что скорость выделения водорода при заданной концентрации и том же потенциале не зависит от рН в околоэлектродгюм лое. [20]
В табл. 9 представлено несколько показательных значений перенапряжений. Существование перенапряжения делает возможным применение платинового катода для определения вольт-амперных кривых таких металлов, как свинец, олово, таллий. Эти металлы выделяются при положительных значениях потенциалов, поскольку после протекания незначительного количества электричества электрод покрывается соответствующим металлом. [21]
К металлам, характеризующимся большим значением перенапряжения ( малой энергией адсорбции водорода), например Hg, Pb, применима теория медленного разряда, при помощи которой можно объяснить большинство явлений, связанных с изменениями перенапряжения водорода. [22]
К металлам, характеризующимся малым значением перенапряжения ( большой энергией адсорбции водорода), например Pt, Ni, наиболее применима теория рекомбинации. [23]
К металлам, характеризующимся малым значением перенапряжения ( большой энергией адсорбции водорода), например к платине, никелю, применима теория рекомбинации. [24]
Этот переход совершается при таком значении перенапряжения ц, при котором сравниваются идеальные энергии активации обычного и безбарьерного разряда. [25]
Из рис. 2.37 видно, что значения перенапряжений в существенной мере зависят от задержки сигнала управления. Поэтому система управления должна иметь малую внутриканальную асимметрию управляющих напряжений. [26]
 |
Зависимость перенапряжения водорода от атомного радиуса металла. [27] |
На рис. 1 - 1 приведено значение перенапряжения выделения водорода для металлов с различным атомным радиусом. [28]
Первый член в правой части уравнения определяет значение перенапряжения при единичной плотности тока ( например, 1 А / см2) и зависит от тока обмена ( ( о) реакции ионы гидроксония - молекулярный водород. Ток обмена в сильной степени зависит от природы металла и уменьшается в ряду Pd, Pt, Fe, Au, Ag, Ni, Си, Т1, Sn, Pb, Hg, что соответствует возрастанию перенапряжения выделения водорода в той же последовательности. Величина 2 3 RT / a F слабо зависит от природы металла и для большинства металлов составляет 90 - 140 мВ, т.е. на такое значение происходит увеличение перенапряжения выделения водорода ( или сдвиг потенциала под током в отрицательную сторону) при возрастании катодной плотности тока в 10 раз. [29]
В табл. 1 в качестве иллюстрации приводятся сравнительные значения перенапряжения т) для разряда ионов различных металлов на ртутном капающем электроде в присутствии молекулярных добавок и трибензи-ламина. [30]
Страницы: 1 2 3 4