Значение - перенапряжение - водород
Cтраница 1
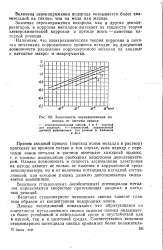 |
Зависимость перенапряжения водорода от чистоты свинца. [1] |
Значение перенапряжения водорода, как и других деполяризаторов, в коррозии металлов вытекает из сущности теории электрохимической коррозии - и прежде всего - кинетики катодной реакции. [2]
Значения перенапряжения водорода в зависимости от металла меняются сильно, влияние изменения электролита относительно невелико. [3]
Если предположение о значении перенапряжения водорода в этом случае справедливо, то, меняя его в пределах 0.6 - 0.8 V, можно получить ряд полимергомологов сальварсана. [4]
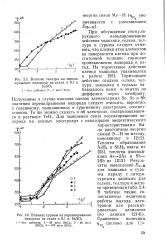 |
Влияние теллура на перенапряжение водорода яа стали в 0 1 н. H2SO4.| Влияние сурьмы на перенапряжение. [5] |
Полученные в случае наличия пленок элементарных Se, As и Sb значения перенапряжения водорода следует относить, вероятно, к селеновому, мышьяковому и сурьмяному электродам, соответственно. [6]
Если в процессе опыта отсасывать с поверхности амальгамы загрязнения, па которых разряжается водород, то можно на 2 - 3 порядка уменьшить скорость разложения амальгамы и получить значение перенапряжения водорода в нейтральном растворе 2 1 с, что, в сравнении с опытами В. С. Багоцкого и И. Е. Яблоковой, на 0 27 в превышает перенапряжение водорода на ртутном катоде. Такое значительное повышение перенапряжения водорода от введения в ртуть небольшого количества щелочного металла объясняется том, что это небольшое количество щелочного металла значительно снижает поверхностное натяжение ртути, а уменьшение поверхностной энергии приводит к ослаблению адсорбционной связи для адсорбированного водорода, концентрация которого вследствие этого понижается, что и приводит к уменьшению скорости разряда водорода. Понижение поверхностного натяжения ртути за счет введения в нее натрия в концентрации 0 1 % по данным разных авторов составляет 100 - 150 дин / см. Сопоставление констант а перенапряжения водорода для различных металлов с поверхностным натяжением показывает, что уменьшение поверхностного натяжения на 1 дин / см увеличивает перенапряжение водорода примерно на 0 8 мо. Таким образом, перенапряжение водорода на 0 1 % - пой амальгаме натрия должно быть выше, чем на ртути примерно па 80 - 120 мв. Более высокое полученное значение объясняется, вероятно, известной неопределенностью этой расчетной величины, а также некоторым влиянием концентрированного раствора. [7]
Это означает, что замедление процесса выделения водорода тем больше, чем слабее данный металл катализирует реакцию молизации атомов водорода. В действительности значение перенапряжения водорода для свинца велико, а каталитическая его активность мала; для платины - наоборот. [8]
В промышленных электролизерах катоды обычно изготавливают из железа или стали, покрываемых никелем или кобальтом для снижения перенапряжения водорода. В табл. 1.2 приведены значения перенапряжения водорода в щелочном электролите для этих катодов, а также ( для сравнения) платинированной платины при нескольких плотностях тока. [9]
Одним из способов изменения скорости реакции катодного выделения водорода является образование на поверхности железа осадков металлов о различным перенапряжением водорода при введении в раствор соответствующих катионов. Осадки платиновых металлов обладают очень низким перенапряжением водорода и переводят реакцию разряда Н в диффузионный режим при потенциалах коррозии железа в фоновых растворах, при этом скорость анодного растворения железа увеличивается в 100 - ш раз. Значение велеча-нн перенапряжения водорода на осадках таких металлов, как Си, ft / i ш J / ty, не намного ниже, чем на железе, поэтому при потенциалах коррозии железа разряд Н протекает на этих осадках в кинетическом режиме. В этом случае скорость анодного растворения железа возрастает в 1 5 - 3 раза. [10]
Металлы IV, V и VI групп периодической системы ( и в первую очередь - титан, цирконий, тантал) характеризуются средним значением перенапряжения водорода. Выделение последнего на этих металлах идет на покрывающих поверхность оксидных пленках, образование которых происходит при достаточно высоких катодных потенциалах. Полупроводниковые и электрокаталитические свойства этих пленок определяют значения перенапряжения водорода. [11]
Аналогично можно построить диаграммы Е - рПдля других элементов. Но для определения получения металлов во многих случаях нужно знать еще значение перенапряжения водорода на выделяемом металле. [12]
Одним из продуктов электролиза в водных растворах во многих случаях является водород, поэтому остановимся на величине перенапряжения водорода. Перенапряжение водорода в значительной степени зависит от металла, на котором он выделяется. Небольшая примесь одного металла к другому может сильно изменять на нем перенапряжение водорода и зависимость перенапряжения от плотности тока. В табл. 22 приведены значения перенапряжения водорода и кислорода на чистых металлах при различных плотностях тока. [13]
Одним из продуктов электролиза в водных растворах во многих случаях является водород, поэтому остановимся на величине перенапряжения водорода. Перенапряжение водорода в значительной степени зависит от металла, на котором он выделяется. Небольшая примесь одного металла к другому может сильно изменять на нем перенапряжение водорода и зависимость его от плотности тока. В табл. 17 приведены значения перенапряжения водорода на разных чистых металлах при трех плотностях тока. [14]
Перенапряжение при выделении кислорода в значительно большей степени зависит от различных, факторов, трудно поддающихся учету. Поэтому экспериментальные данные по кислородному перенапряжению, полученные разными авторами, заметно расходятся между собой. Зависимость кислородного перенапряжения от плотности тока обычно не может быть выражена простой формулой, как в случае водородного перенапряжения. В таблице 4 приведены значения перенапряжения водорода и кислорода на некоторых металлах в щелочных растворах. [15]
Страницы: 1 2