Реакция - образование - ацетон
Cтраница 2
Как следует из рис. 196, концентрация катализатора ( НВг) устанавливается неизменной с некоторого момента реакции, процесс же образования ацетона в системе продолжается со значительной скоростью. Это, а также и некоторые другие основания приводят авторов к заключению, что НВг по отношению к реакции образования ацетона является истинным катализатором и, следовательно, катализ бромистым водородом связан лишь с очень небольшой его затратой. Основной же расход НВг осуществляется по параллельной реакции образования броморганических соединений. [16]
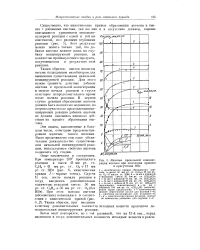 |
Явление предельной концентрации ацетона при окислении пропана в присутствии НВг. [17] |
Таким образом, ацетон является весьма подходящим ингибитором для выявления существования начальной инициирующей реакции. Для этого нужно сравнить действие добавок ацетона в предельной концентрации в момент начала реакции и спустя некоторое непродолжительное время после начала реакции. В первом случае реакция образования ацетона должна быть полностью подавлена; во втором случае после прохождения инициирующей реакции добавка ацетона не должна оказывать никакого действия на процесс образования ацетона. [18]
Активным катализатором для этих реакций, впервые предложенным Сабатье [264], может служить металлическая медь, которая, однако, быстро утрачивает каталитическую активность. Активные катализаторы также мо гут быть получены на основе никеля и платины, но такие контакты вызывают последующее разложение образующихся альдегидов и кетонов. Катализатором этой реакции, а также реакции образования ацетона из изопропилового спирта при 600 - 620 является латунь, обеспечивающая количественный выход указанных продуктов. [19]
Для этого необходимо добавить предельное количество ацетона в одном опыте в момент начала реакции, а в другом опыте спустя небольшое время после начала реакции. Если инициирующая реакция действительно имеется и ацетон ее ингибирует, то в первом опыте образование ацетона должно быть полностью подавлено; во втором же, в котором ацетон был добавлен после прохождения инициирующей реакции, его добавка не должна сказаться на реакции образования ацетона. [20]
Таким образом, были получены кинетические кривые накопления промежуточного инициатора при разных температурах. Полученные кривые имеют S-образный характер. Это указывает на то, что образование промежуточного инициатора является ценным разветвленным процессом. Образование промежуточного инициатора прекращается, когда в системе еще имеются значительные концентрации всех трех исходных веществ: пропана, кислорода и НВг. Следовательно, начальная инициирующая стадия является самотормозящимся процессом. Эта величина значительно отличается от энергии активации реакции образования ацетона ( 25 ккал), что также указывает на резко отличную природу обоих процессов. [21]
Далее нами было показано, что, приготовил смесь из пропана, кислорода, бромистого водорода и ацетона в соотношениях, отвечающих концу реакции, мы можем полностью подавить реакцию образования ацетона. В наглядной форме это явление представлено на рис. 15, из которого видно, что чем больше ацетона прибавлено к исходной смеси пропана, кислорода и бромистого водорода, том меньше образуется этого продукта в ходе реакции. НВг процесс образования ацетона подавляется полностью. Если бы предел был связан с термодинамическими соотношениями между компонентами реакции, то можно было бы ожидать, что при добавках ацетона выше предельной концентрации мы наблюдали бы постепенное уменьшение количеств ацетона до предельной. Введя в исходную смесь добавку ацетона, равную 100 мм рт. ст., мы определили анализом, что в реакционном сосуде содержится именно это количество ацетона независимо от времени пребывания смеси. Следовательно, нужно допустить, что в качестве продуктов, затормаживающих реакцию образования катализирующего продукта /, выступает не только ацетон ( которого в начале процесса еще мало), но также и другие вещества. Эти же вещества могут останавливать реакцию бромирования, которая не тормозится добавками ацетона, даже в предельных концентрациях. Добавки ацетона приводят к уменьшению J0 - концентрации катализирующего вещества /, которой она достигает к концу процесса создания этого вещества. Опыты с добавками ацетона в продельных концентрациях еще раз убеждают нас, что по отношению к реакции образования ацетона бромистый водород выступает как истинный гомогенный катализатор. [22]
Страницы: 1 2