Реакция - разложение - амальгама
Cтраница 1
Реакция разложения амальгамы водой протекает довольно медленно. [1]
 |
Схема горизонтального ( а и вертикального ( б диффузионных электролизеров с диафрагмой. [2] |
Таким образом, ингибирующее действие этих веществ в реакции разложения амальгамы можно объяснить тем, что металлы, присутствующие в системе и вызывающие каталитический разряд водорода, лучше смачиваются амальгамой. Разумеется, в отдельных случаях механизм ингибирования может быть иным. [3]
Невольно напрашивается вопрос, нельзя ли использовать энергию реакции разложения амальгамы для получения электрической энергии и компенсировать этим часть затрат на электролиз поваренной соли. [4]
Эта разность температур, как известно, возникает за счет теплового эффекта реакции разложения амальгамы натрия, а также теплового эффекта разбавления каустика. [5]
Теоретическое истолкование найденной Бренстедом и Кейном необычной кинетической зависимости было дано Фрумкиным [13], который предложил рассматривать реакцию разложения амальгам как электрохимический процесс, скорость которого определяется скоростью разряда ионов водорода при потенциале разлагающейся амальгамы. [6]
 |
Хлорный цех. [7] |
Амальгаму разлагают в аппарате, отделенном от электролизера и называемом разлагателом. Однако реакция разложения амальгамы протекает в отсутствие хлорида и образующаяся щелочь не содержит примесей, препятствующих ее применению в производство вискозы и других областях. Кроме того, концентрация щелочи, полученной при разложении амальгамы, значительно выше концентрации продукта, получаемого в диа-фрагменном электролизере. [8]
 |
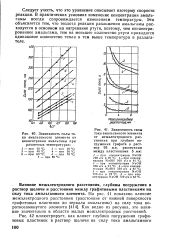
Изменение УС амальгамы во времени ( время на оси абсцисс в мин при разложении амальгам щелочных металлов в 1 0 N водных растворах их гидроокисей, содержащих 1 0 моль / л ацетона. [9] |
Такого же типа зависимости получены для нейтральных и кислых сред. Сопоставление опытных констант скоростей реакций разложения амальгамы в кислых ( рН 3 - 5) и щелочных ( рН 13) растворах в присутствии некоторых кетонов, в частности ацетона, показывает, что этот процесс протекает по электронному механизму, так как повышение концентрации ионов водорода в растворе не приводит к увеличению скорости разложения амальгам. [10]
В щелочных растворах авторы отмечают плохую воспроизводимость экспериментальных данных. Как следует из приводимых в статье результатов, реакция разложения амальгамы натрия в общем подчиняется уравнению (4.1), однако константы скорости, полученные на основании различных опытов, сильно отличались друг от друга. [11]
В опыте с амальгамированием железной проволочки в растворе, содержащем Са2, было найдено, что введопие поверхностно-активного вещества ускоряет амальгамирование железа. Таким образом, ингибирующее действие этих поверхностно-активных веществ в реакции разложения амальгамы следует объяснять улучшением смачивания амальгамой присутствующих каталитических металлов. [12]
Для выяснения природы амальгамного гидрирования органических соединений вопросом первостепенной важности является выяснение механизма выделения водорода при разложении амальгам. В 30 - е годы А. Н. Фрумкин [24], рассматривая реакцию разложения амальгам щелочных металлов как типичный электрохимический процесс, скорость которого лимитируется скоростью разряда ионов водорода при потенциале амальгамы, объяснил найденную Дж. [13]
Однако в результате получается весьма громоздкое уравнение, пользоваться которым для расчета скорости реакции разложения амальгамы неудобно. Интегрирование уравнения (4.35) значительно упрощается, если ввести некоторые допущения. Рассмотрим два наиболее вероятных случая. [14]
Страницы: 1 2