Реакция - взаимодействие - аммиак
Cтраница 2
Поэтому нет нужды делать количественный расчет констант равновесия реакций взаимодействия аммиака с уксусной и более высокомолекулярными кислотами, так как и без расчета ясно, что и в этом случае реакции образования нитрилов из аммиака и жирных кислот при атмосферном давлении и температурах порядка 300 - 1000 К будут протекать практически до конца. [16]
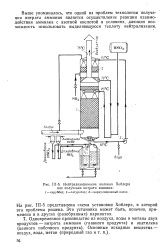 |
Нейтрализационная колонна Хоблера. [17] |
Выше упоминалось, что одной из проблем технологии получения нитрата аммония является осуществление реакции взаимодействия аммиака с азотной кислотой в условиях, дающих возможность использовать выделяющуюся теплоту нейтрализации. [18]
По мнению Пирсона [212-214], каталитическое влияние хромита и хромата меди при горении топлив обусловлено промотированием реакции взаимодействия аммиака или олефинов с хлорной кислотой. Кроме того, скорость горения увеличивается за счет выделения тепла от реакции на катализаторе. Последнее заключение в свете данных по измерению температур [93, 101] не кажется нам правдоподобным. [19]
Например хлористый этилен может реагировать с водным аммиаком при 110 с образованием1 этилен-диамина без применения катализатора, хотя медь или некоторые другие металлы, следующие в ряду напряжения за водородом, нужны при реакции взаимодействия аммиака с соединениями, содержащими галоид, присоединенный к бензольному ядру, например с хлорбензолом, 4-хлор - 2-фенилантрахиноном, хлорбензоилбенэой-ной кислотой. Эти исследователи отмечают также, что прибавление азотнокислого аммония или таких окислителей, как хлорат калия, к соединениям меди повышает выход и чистоту получаемых аминов. Это имеет особое значение для аминирова-ния соединений, содержащих галоид в бензольном ядре. В противоположность выводам Hale и Britton a 35b в их работе с анилином Grogginsi и Stirton нашли, что присутствие металлической меди в тех случаях, когда соединения меди применяются в качестве катализатора, не является необходимым, точно так же как не имеется никаких преимуществ в применении восстановленной меди - л качестве катализатора. [20]
При абсорбции аммиака и оксида углерода ( IV) рассолом иыдилястся большое количество тепла. Кроме того, реакция взаимодействия аммиака и оксида углерода ( IV) сопровождается выделением тепла. Тепло также - выделяется при конденсации водяных паров. Общего количества тепла достаточно для нагревания рассола на 80 - 90 С. Поскольку при повышении температуры процесс абсорбции аммиака ухудшается, абсорбцию ведут с промежуточным охлаждением жидкости в холодильниках. [21]
Присоединение веществом кислорода ( или отнятие от него водорода) называется окислением. Реакция взаимодействия аммиака с кислородом также является реакцией окисления, так как водород отнят от вещества, в результате чего образовались азот и вода. [22]
Для просушки используются сушильные барабаны 10, 13 пальмеровского типа. Каждый из них состоит из большого нагревательного барабана И, вокруг которого наматывается просушиваемая ткань; оба барабана соединены последовательно. В соответствии с технологией реакция взаимодействия аммиака с тканью практически прекращается при устаиовленни контакта ткани с первым барабаном. [23]
Последние приписывали активирование реакции образованию ионов, возникающих в первичной реакции и адсорбируемых инертными молекулами, которые они активируют, давая высокий количественный выход. Бакер [36] предполагал, что ионные ядра с высокой удельной индуктивной способностью образуются водой, конденсируемой на ионах и электронах как центрах реакции. Было также высказано предположение, что центры реакции являются группами ионов, как это иллюстрируется реакцией взаимодействия аммиака и хлористоводородной кислоты, ион Н3О ( гидратированный водород) и ион С1 окружаются слоем молекул аммиака. [24]
Какое значение имеет азот для животных и растений. Как получают и где применяют азот. Перечислить свойства азота: а) физические, б) химические. Какие соединения образует азот с кислородом ц какая в них валентность азота. Сколько хлористого аммония взаимодействует с 28 г окиси кальция при получении аммиака. Сколько гидроокиси кальция взаимодействует с 10 7 г хлористого аммония при получении аммиака. Написать уравнения реакций взаимодействия аммиака с кислотами: а) соляной, б) азотной, в) серной, г) угольной, д) фосфорной; назвать образующиеся при этом вещества. [25]
Страницы: 1 2