Реакция - хинолин
Cтраница 1
Реакция хинолина с хлорноватистой кислотой приводит к образованию 2-оксихинолина [422] ( стр. [1]
При реакции 2-замещенного хинолина с алкиллитием в одном случае было отмечено замещение группы, находящейся в положении 2 хинолина, алкильной группой реагента. Если подействовать я-бутиллитием на 2-этоксихинолин и полученный продукт подвергнуть карбонизации и гидролизу, то образуется 2-и-бутилхинолин - и 2-этоксихинолин - З - карбоновая кислота. [2]
Механизм реакции хинолина с бромистым цианом не вполне ясен. По данным Брауна [772], первоначально происходит взаимодействие с азотом цикла, после чего имеет место перегруппировка. Однако промежуточный продукт изучен лишь частично. [3]
Таким образом, реакции хинолина и изохинолина с электрофильными реагентами протекают по бензольному кольцу, в то время как реакции с нуклеофильны-ми реагентами - по пиридиновому. [4]
Циглер и Цейзер [762] получили смесь 2-н-бутил - и 4-н-бутилхи - нолинов при реакции хинолина с я-бутиллитием. При использовании фенил-лития 2-фенилхинолин образуется наряду с соединением, относительно-которого предположили, что оно является 4-фенилхинолином. Гильман и Гэйнер [763] повторно исследовали реакцию между фениллитием и хино-лином и получили 2-фенилхинолин, а также вещество, которое оказалось 2 2-дифенил - 1 2-дигидрохинолином. Доказательство структуры этого вещества основывается на том, что идентичные соединения образуются как при присоединении фениллития к 2 - ( / 1-толил) хинолину, так и при присоединении п-толиллития к 2-фенилхинолину. [5]
Однако, как это будет показано далее, нельзя, исходя из сказанного, объяснить все реакции хинолина. В частности, заместители в положении 5 часто неожиданно проявляют аномальную лабильность. [6]
Однако, как это будет показано далее, нельзя, исходя из сказанного, объяснить все реакции хинолина. В частности, заместители в положении 5 часто неожиданно проявляют аномальную лабильность. [7]
Напишите реакции хинолина со следующими соединениями: а) соляной и серной кислотами на холоду; б) йодистым метилом; в) нитрующей смесью; г) амидом натрия. В какое положение вступают замещающие группы и почему. [8]
При гидролизе продуктов присоединения образуются вторич ные амины. При гидролизе продуктов реакции хинолина с диизобутилалюминийгидридом получается 1 2-дигидрохинолин, аналогичным образом из изохинолина получается 1 2-дигидро-изохинолин, который восстанавливается далее до 1 2 3 4-тетра-гидроизохинолина. [9]
Хотя и было сделано много попыток уяснить поведение хинолина в таких реакциях, как нитрование и сульфирование, имеющихся данных недостаточно для окончательных выводов. Гьюизген [810] сопоставил многие реакции хинолина с аналогичными реакциями нафталина. Для нафталина не существует причин, чтобы a priori признать существование фиксированных двойных связей в одном кольце; точно так же и для хинолина нет оснований утверждать, что фиксированные двойные связи имеются в бензольном кольце. Однако, как будет показано ниже, наличие фиксированных двойных связей более вероятно в бензольном кольце хинолина, чем в кольце нафталина. Другими словами, многие реакции хинолина и его замещенных производных полностью согласуются с представлением о фиксированной сопряженной диеновой системе двойных связей в бензольном кольце. [10]
Данную реакцию интересно сравнить с реакцией хинолина с хлористым бензоилом в присутствии основания, при которой происходит раскрытие цикла ( стр. Этот же дихинолин был, невидимому, получен Вейделем [1038] при сухой перегонке цинхониновой кислоты с гидратом окиси кальция, Бесторном и Ибелом [1034] при сухой перегонке хинальдиновой кислоты, Спади [1039] при сухой перегонке 3-изопропилхинальдиновой кислоты, Циммерманом и Мюллером [1040] при пропускании паров хинолина через раскаленную докрасна железную трубку и Фишером и ван Лоо [1041] при сухой перегонке хинолин-8 - сульфокислоты. [11]
Это соединение было также получено в качестве побочного продукта при реакции хинолина с амидом натрия ( стр. [12]
Катализатор, на котором хинолин адсорбировался при такой высокой температуре, был окрашен в бледнозеленый цвет. При кипячении обработанного хинолином катализатора с водным раствором соляной кислоты образуется раствор, содержащий большую часть хинолина. Эти наблюдения подтверждают предположение о том, что катализатор удерживает непосредственно хинолин, а не продукты его распада. Результаты исследования реакций хинолина с катализаторами крекинга-свидетельствуют о том, что каталитическая активность связана с кислотными свойствами катализатора. Было найдено, что сила катализаторов различного строения и различной активности пропорциональна количеству хинолина, которое они способны химически адсорбировать. Кроме того, было установлено, что в результате хемосорбции хинолина происходит отравление катализатора. [13]
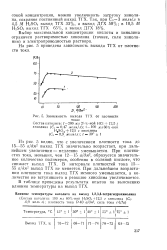 |
Зависимость выхода ТГХ от плотности. [14] |
Из рис. 5 видно, что с увеличением плотности тока до 15 - 55 а / дм2 выход ТГХ значительно возрастает, при дальнейшем увеличении - медленно уменьшается. При плотностях тока, меньших, чем 12 - 15 а / дм2, образуется значительное количество полимеров, особенно в соляной кислоте, что снижает выход ТГХ. В интервале плотностей тока 15 - 55 а / дм2 выход ТГХ не меняется. При дальнейшем возрастании плотности тока выход ТГХ немного уменьшается, а количество не вступившего в реакцию хинолина увеличивается. [15]
Страницы: 1 2