Реакция - хром
Cтраница 1
Реакция хрома с тетрафторидом урана протекает непрерывно, лишь до тех пор, пока не наступит равновесие. Никель очень сильно поглощает нейтроны и не может широко применяться в активной зоне реактора для отделения ее от зоны воспроизводства, а также для покрытия графитового замедлителя. Большинство сортов графита имеет слишком большую пористость и сорбирует значительное количество солей, но с целью использования для фторидных расплавов разработан специальный сорт непроницаемого графита. Такой графит может служить для разделения активной зоны и зоны воспроизводства, а также в качестве замедлителя, не требующего покрытия. [1]
Реакция хрома ( III) с ЭДТА особенно полезна, когда хром является основным компонентом в таких минералах, как хромит, но ее с успехом используют также для некоторых пород и силикатных минералов, содержащих 1 % и более хрома. Предел, ниже которого необходимо предварительное отделение кремнезема, по-видимому, составляет около 0 2 % Сг; при содержании Сг ниже 0 5 % лучше пользоваться фотометрическим методом, основанным на измерении интенсивности желтой окраски растворов щелочного хромата. [2]
Ниже рассматриваются реакции хрома, кремния, марганца, титана, углерода, серы, фосфора и других примесей при сварке аустенитных сталей и сплавов. Одновременно излагаются основные соображения о построении флюсов-шлаков для сварки аустенитных сталей и сплавов. [3]
Молярный коэффициент погашения продукта реакции хрома ( УТ) с дифенилкарбазидом составляет, согласно Аллену [42], 4 17 - Ю1 ( удельное поглощение 0 80) при Ямакс 546 нм. [4]
Уран не влияет на реакцию хрома с дифенилкарбазидом. [5]
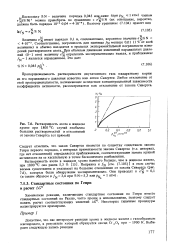 |
Растворимость азота в жидком хроме при 1800 С. случай необычно больших растворимостей и отклонений от закона Сивертса ( от прямой. [6] |
Допустим, что нас интересует реакция хрома в жидком железе с газообразным кислородом, в результате которой образуется оксид Cr 2 О, при - 1900 К. [7]
Механизм этой реакции подобен механизму реакции хрома ( У1) с дифенилкарбазидом ( см. стр. Фиолетовый комплекс рения экстрагируется хлороформом. Молярный коэффициент погашения составляет 2 04 - 10 при Ямакс - - 545 нм. [8]
 |
Химический состав летучей золы бурых углей, %. [9] |
При температурах выше 450 С интенсивность реакции хрома со щелочными хлоридами существенным образом увеличивается. [10]
Так как описываемые ниже методы основаны на реакциях хрома ( VI), то необходимо, чтобы хром был полностью окислен. Поэтому перед выполнением определения хром окисляют персульфатом аммония в сернокислой среде. [11]
Аналогичные термодинамические расчеты [ 10, И ] процесса хлорирования феррохрома показали, что изобарные потенциалы реакций хрома и железа с хлором имеют большие отрицательные значения; наиболее вероятно образование хлоридов трехвалентных металлов. Хлорирование феррохрома сопровождается сильным выделением тепла, причем тепловой эффект реакций мало изменяется с температурой. Повышение температуры вызывает уменьшение константы равновесия, но ее значение достаточно велико даже при высокой температуре. [12]
С использованием радиоактивного 14С, введенного в аустенитную нержавеющую сталь с 18 % Сг, 12 8 % Ni, 0 12 % С, установлено, что сразу после закалки стали от 1000 - 1350 С на границах зерен повышается содержание углерода. Это указывает, что период сенсибилизации может зависеть не только от времени, необходимого для диффузии добавочных количеств углерода к границам зерен, но отчасти и от скорости реакции хрома с углеродом, уже существующим на границе зерен. [13]
Трубка закрепляется в горизонтальном положении; ее нагревание производят горелкой с воздушным дутьем. Затем усиливают нагревание, поднимая температуру до максимально достижимой, охлаждают и вытесняют хлор сухим CCV В трубке образуется СгС13 в виде блестящих фиолетовых листочков, причем объем образовавшегося твердого вещества значительно превышает объем взятого для реакции хрома. Для того чтобы избежать возможности забивания трубки, рекомендуется при загрузке хрома распределить его по длине трубки. [14]
По своему химическому поведению молибден и вольфрам гораздо сильнее отличаются от хрома, чем между собой. Например, в отличие от хрома степень окисления 3 для молибдена и вольфрама реализуется лишь в небольшом числе катионных комплексов. Реакции хрома ( III) во многом сходны с реакциями железа ( III) и алюминия. [15]
Страницы: 1 2