Реакция - гашение - известь
Cтраница 1
Реакция гашения извести является обратимой реакцией. [1]
Когда реакция гашения извести закончится, шипение и разбрызгивание массы прекратится, добавить из цилиндра воды до половины чашки, размешать и перенести полученную массу стеклянной палочкой в стакан емкостью 250 - 300 мл. Перенести в стакан всю воду из цилиндра, обмыв ею при этом несколько раз чашку и стеклянную палочку. Добавить в стакан еще 50 мл воды, хорошо размешать полученную суспензию гидроксида кальция и дать ей отстояться. [2]
Теплота реакции гашения извести составляет 66 94 кДж / моль. [3]
 |
Прибор для получения и очистки диоксида углерода.. - аппарат Киппа. 2 3 - склянки Тищенко. 4 -колба ( приемник. [4] |
По окончании реакции гашения извести ( прекращение шипения и разбрызгивания массы) добавляют из цилиндра воду до половины чашки, размешивают стеклянной палочкой и помещают полученную массу в стакан. Тщательно обмывают водой из цилиндра чашку и палочку и переносят в стакан. Добавив в стакан еще 5О мл воды, размешивают полученную суспензию гидроксида кальция и дают ей отстояться. Проверяют реакцию среды красной лакмусовой бумагой. [5]
Исследована скорость реакции гашения извести с получением концентрированного известкового молока в области температур 60 - 95 для извести с размером кусков от 7 до 55 мм. [6]
Если, например, реакция гашения извести протекает в замкнутом сосуде, то реагирующую массу вещества в этом случае следует рассматривать как систему, а реакционный сосуд и охладитель - как внешнюю среду. [7]
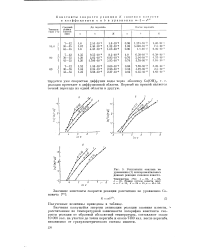 |
Результаты анализа по уравнению ( 1 экспериментальных данных реакции гашения извести. [8] |
Значения кажущейся энергии активации реакции гашения извести, рассчитанные по температурной зависимости логарифма константы скорости реакции от обратной абсолютной температуры, составляют около 10 000 кал. [9]
Установлено, что в начальной стадии реакция гашения извести водой лежит в кинетической области, а после достижения степени загасни 0.5 - 0.6 переходит в диффузионную или диффузионно-кинетическую область. [10]
Данный прием не рекомендуется применять в младших классах. Практика показывает, что учащиеся в этом случае не столько обращают внимание на сам процесс гашения извести, сколько на горение спирта. В ответах на следующем уроке учащиеся обычно подробно рассказывают о горении спирта, но забывают, что реакция гашения извести проходила с выделением тепла. [11]
Гашение извести сопровождается выделением значительного количества теплоты. Выделяющаяся теплота вызывает кипение воды, поэтому негашеную известь называют кипелкой. По окончании реакции температура смеси снижается. Момент начала снижения температуры смеси является признаком прекращения реакции гашения извести. В процессе гашения комовой извести некоторая ее часть может либо вообще не погаситься, либо гаситься очень медленно. [12]
Страницы: 1