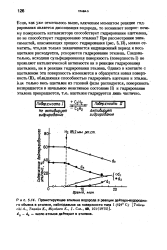
Реакция - гидрирование - ацетилен
Cтраница 1
Реакция гидрирования ацетилена солями хрома и реакция окисления его солями осмия препятствуют реакции получения ацетиленидов этих металлов. [1]
Аналогичное строение было предложено для переходного комплекса реакции гидрирования ацетилена. [2]
Сколько литров водорода требуется для получения 134 л этана при реакции гидрирования ацетилена. [3]
Установлено, что на никелевых, палладиевых и платиновых катализаторах реакция гидрирования ацетилена до этана имеет нулевой порядок по ацетилену и первый по водороду. Однако в литературе отсутствуют надежные данные о кинетике реакции гидрирования NO на катализаторах платиновой группы. [4]
Взаимодействие NiCl с HG1 приводит к образованию NiGb и H. Последний и участвует в реакциях гидрирования ацетилена и акриловой кислоты. [5]
Это слагаемое, как он указывает, должно быть равно или кратно величине энергии связи между атомами металла. Приводя расчеты соответствующих величин для реакции гидрирования ацетилена [1195] и изотопного обмена водорода с дейтерием [542], Ландау рассматривает их как подтверждение развиваемой точки зрения. [6]
Изучалась кинетика парофазного гидрирования метилацетилена в статической системе интервале 20 - 230 С в присутствии различных порошкообразных и нанесенных на пемзу катализаторов: никеля, кобальта, железа, родия, иридия, осмия, платины, меди, а также на никель-медных сплавах разного состава. Результаты сходные с полученными ранее для реакции гидрирования ацетилена, обсуждены в аспекте влияния электронной структуры на каталитические свойства металлов и сплавов. [7]
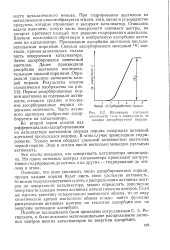 |
Изменение удельной. [8] |
При гидрировании ацетилена на металлическом никеле образуется этилен, этан, метан и углеродистые продукты, которые отравляют и засоряют катализатор. Ставилась задача выяснить, какую часть поверхности занимают центры, на которых протекает каждый тип реакции гидрирования ацетилена. [9]
Если, как уже отмечалось выше, ключевым моментом реакции гидрирования является диссоциация водорода, то возникает вопрос: почему поверхность катализатора способствует гидрированию ацетилена, но не способствует гидрированию этилена. При рассмотрении зависимостей, описывающих процесс гидрирования ( рис. 5.13), можно отметить, что как только заканчивается индукционный период и весь ацетилен расходуется, ускоряется гидрирование этилена. Следовательно, исходная сульфидированная поверхность ( поверхность I) не проявляет каталитической активности ни в реакции гидрирования ацетилена, ни в реакции гидрирования этилена. Однако в контакте с ацетиленом эта поверхность изменяется и образуется новая поверхность ( П), обладающая способностью гидрировать ацетилен и этилен. Как только весь ацетилен из газовой фазы расходуется, поверхность возвращается в начальное неактивное состояние ( I) и гидрирование этилена прекращается, т.е. ацетилен-гидрируется лишь частично. [11]
Соединения хрома могут быть использованы в электролизере с диафрагмой для одновременного окисления одного вещества на аноде и восстановления другого на катоде. Ионы Сг2, отдавая электроны, восстанавливают вещество, находящееся в катодном пространстве. Таким методом в США осуществляют процесс одновременного восстановления азоксибензола в бензидин и окисления антрацена в антрахинон. Примером восстановления органических соединений в присутствии ионов двухвалентного хрома может служить также реакция гидрирования ацетилена в этилен. [12]
Страницы: 1