Реакция - горение - окись - углерод
Cтраница 2
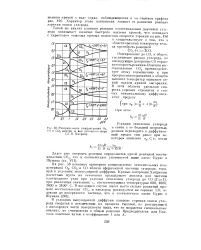 |
Распределение концентраций 02. [16] |
Характер этого понижения зависит от развития реакции горения окиси углерода. [17]
Для процесса горения твердого топлива безусловный интерес представляют реакции горения окиси углерода и водорода. Для твердых топлив, богатых летучими веществами, в ряде процессов и технологических схем необходимо знать характеристики горения углеводородных газов. Механизм и кинетика гомогенных реакций горения рассмотрены в гл. Кроме указанных выше вторичных реакций, перечень их следует продолжить гетерогенными реакциями разложения углекислоты и водяного пара, реакцией конверсии окиси углерода водяным паром и семейством реакций метанообразования, которые с заметными скоростями протекают при газификации под высоким давлением. [18]
Типичным примером гомогенного положительного катализа является влияние водяного пара на реакцию горения окиси углерода с кислородом. Если окись углерода совершенно сухая, то зажженное пламя сейчас же гаснет. В сыром воздухе, напротив, окись углерода горит очень хорошо. Водяной пар здесь является катализатором горения. Так как водяной пар значительно легче распадается на радикалы ( энергия расщепления водяного пара 118 ккал-моль-1, а окиси углерода 160 - 200 ккал-моль -), то реакция может идти при более низких температурах. [19]
Имеются попытки решения этого вопроса путем воздействия на процесс горения ингибиторами, тормозящими реакцию горения окиси углерода. Например, Мертенс [202], Артур [211], применяя различные добавки, такого рода, как иод, СС14, Р205 и др., вводимые совместно с воздухом, достигли при окислении углерода в слое значительного выхода окиси углерода, что дало им основание утверждать первичность образования этого окисла. Мейера, не могут быть пока опровергнуты посредством исследований суммарного процесса горения в слое даже с помощью ингибиторов, которые, кстати, могут влиять не только на реакцию горения окиси углерода, но и на реакцию окисления. [20]
Но вследствие уменьшения скорости v0 при одной и той же длине кислородной зоны роль реакции горения окиси углерода возрастает, что и объясняет ухудшение состава газа в конце кислородной зоны. [21]
 |
Механизация подачи, взвешивания и загрузки шихты в вагранку. [22] |
Подогрев дутья в современных вагранках осуществляется за счет использования физического тепла отходящих газов, теплоты реакции горения окиси углерода. Температура дутья достигает 400 - 500 С. [23]
Наоборот, вещества, связывающие водород ( бром, иод и др.), тормозят реакцию горения окиси углерода и являются так называемыми ингибиторами. [24]
Опыты Цухановой [113] по исследованию горения угольного канала с добавками к кислороду паров иода, тормозящего реакцию горения окиси углерода, привели к выводу об отсутствии заметного влияния реакции 2СО - J - 02 2С02 на расходование кислорода, что объясняется, по-видимому, интенсивным догоранием окиси углерода непосредственно вблизи реакционной поверхности стенок канала. Цуханова указывает, что при этом происходит как бы уменьшение диаметра канала на толщину зоны догорания окиси углерода. На наш взгляд, можно более реально объяснить этот факт. При отсутствии добавки ингибитора ( иода) окись догорает интенсивнее и кислорода поступает к поверхности угольной стенки меньше ( так называемое тормозящее действие пламени СО, рассмотренное нами в гл. В случае же добавки ингибитора окиси догорает меньше, меньше затрачивается кислорода и соответственно меньше сказывается тормозящее действие догорания окиси углерода, в связи с чем кислорода к стенке поступает больше, чем в первом случае. Этим и объясняется отсутствие изменения расходования кислорода, а следовательно, и влияние горения СО вблизи стенки. [25]
Следующая реакция, к которой была применена и на которой проверялась теория цепных разветвленных реакций Н. Н. Семенова, была реакция горения окиси углерода в присутствии небольших количеств Н2, Н20 или других веществ, способных служить донорами водорода. [26]
Большие значения констант равновесия реакций С -) - 02С02 и 2С - - 02 - 2СО при всех температурах показывают, что эти реакции практически протекают до конца в прямом направлении. Реакция горения окиси углерода 2СО - f - 02 2С02, так же как и реакции полного и неполного горения углерода, практически идет полностью в прямом направлении. [27]
Следует заметить, что роль реакции горения окиси углерода в процессе горения и газификации топлива еще недостаточно изучена. Одним из средств для изучения хода реакции горения окиси углерода в слое являются ингибиторы ( см. гл. Применяя ингибиторы, Мертенс [202] сделал вывод о первичном образовании окиси углерода. Восстановление С02 при этом вовсе не учитывается. Как видно из этой схемы, образование СО и последующее его догорание являются последовательными ( так называемыми консекутивными) реакциями. [28]
В 1 разделе данной главы был рассмотрен процесс горения в угольном канале при наличии одной химической реакции - окисления. В действительности этот процесс сопровождается и вторичными реакциями: реакцией восстановления углекислоты и реакцией горения окиси углерода. [29]
Вызывает также сожаление, что в монографии, носящей название Спектроскопия и теория горения, спектроскопические исследования мало связаны с вопросами кинетики и механизма цепных реакций, являющимися центральными вопросами теории горения. В настоящее время мы имеем экспериментально обоснованные ( причем в значительной мере именно благодаря спектроскопическим измерениям) детальные схемы химического механизма ряда реакций горения, в том числе реакции горения окиси углерода, которой Гейдон уделяет большое внимание в своей монографии; имеем общие представления о природе активных центров и основных чертах механизма других реакций, в частности реакций горения углеводородов; имеем, далее, данные по спектрокинетическому и по другим физико-химическим методам анализа ряда окислительных реакций и реакций горения. Результаты всех этих многочисленных исследований либо вовсе не нашли себе места в монографии, либо представлены в ней в виде отрывочных сведений. Между тем, спектроскопические исследования в области химических реакций не являются самоцелью и своей главной задачей имеют решение тех или иных химических вопросов. [30]
Страницы: 1 2 3