Реакция - горение - водород
Cтраница 3
Примером разветвленной цепной реакции является реакция горения водорода. [31]
Справедливость этой формулы в случае реакции горения водорода была экспериментально доказана Ковальским, который показал, что в начале реакции, когда выгорание исходных веществ еще невелико, In Ар является линейной функцией времени. Различными авторами формула вида (43.22) была экспериментально установлена для этой и для других реакций. [33]
Составим, например, уравнение реакции горения водорода на воздухе с образованием воды. Известно, что молекулы водорода и кислорода состоят из двух атомов. [34]
Такой же низший предел давления имеет реакция горения водорода. Эти особенности наблюдаются лишь выше 540; ниже этой тем-лературы реакция идет не цепным путем, а обычным контактным катализом и течение ее мало зависит от давления. [35]
Примером разветвленной цепной реакции может служить реакция горения водорода. [36]
Коэффициент 9 вводится потому, что по реакции горения водорода водяного пара получается по массе в девять раз больше, чем израсходовано водорода. Иногда бывает необходимо учитывать также водяные пары, вносимые в топку с паровым дутьем, если таковое имеется. [37]
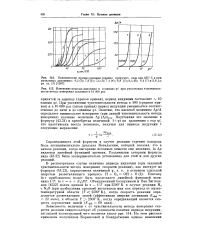
Таким образом, исходя из цепного механизма реакции горения водорода, удается объяснить все особенности этой реакции. Опыт показывает, что разветвленные цепные реакции, кроме двух указанных пределов давления Рг и Р2, имеют еще и третий предел Р3 ( кривая CD на-рис. Последний в большинстве случаев имеет тепловую природу, поскольку при больших давлениях создаются условия, при которых даже при сравнительно медленной вначале цепной реакции скорость выделения тепла превышает скорость его отвода ( 7ВЫД ] 7 тв) из-за чего изотермичность процесса нарушается и наступает воспламенение. [38]
Из реакций горения других веществ укажем на реакцию горения водорода и серы. [39]
К числу гомогенных реакций относятся, например, реакции горения водорода и окиси углерода и реакция конверсии окиси углерода; к числу гетерогенных - реакции полного и неполного горения углерода, восстановления углекислоты и разложения водяного пара. [40]
Отсюда можно заключить, что твердая поверхность способствует возникновению реакции горения водорода и тормозит уже идущую реакцию. [41]
При высоких давлениях ( выше верхнего предела Р Р2) механизм реакции горения водорода оказывается иным - реакция становится простой ( неразветвленной) цепной реакцией. При высоких давлениях тройные столкновения в системе преобладают над двойными, вследствие чего реакции разветвления цепи ( V33), (V.34) утрачивают свое значение - затухают. [42]
 |
Зависимость скорости разветвленной цепной реакции от времени. [43] |
Это доказывает, что гидроксил и атомарный водород являются основными активными центрами реакции горения водорода. [44]
Однако закон действующих масс и уравнение Аррениуса недостаточны для объяснения истинного характера протекания реакций горения водорода, углерода и его окиси. [45]
Страницы: 1 2 3 4