Реакция - горение - углеводород
Cтраница 1
Реакция горения углеводородов протекает более сложно, чем горение водорода или окиси углерода. Первая реакция протекает медленно, причем температура повышается также медленно. Возникновение индукционного периода связано с тем, что наряду с образованием происходит и обрыв цепей, что тормозит протекание реакции. [1]
Кинетика реакций горения углеводородов по сравнению с рассмотренными реакциями окисления водорода и окиси углерода более сложна. [2]
Вода накапливается из-за испарения остаточной воды и реакции горения углеводородов. Перед зоной конденсации образуется вал легких углеводородов и воды, конденсирующихся из паров легких фракций нефти и воды. [3]
Найденные для гремучей смеси закономерности и факты затем подтверждены и обобщены на реакциях горения углеводородов, методом фиксации промежуточных перекисей и альдегидов при низких температурах. [4]
Дискуссия об ацетилене, который, по мнению Андерсона [17], является промежуточным продуктом в реакции горения углеводородов. Рассмотрен как пиролитический, так и окислительный аспекты процесса образования и горения ацетилена. [5]
Спектроскопическими исследованиями было показано, что, так же как и в случае окисления Н2 и СО, в зоне реакции горения углеводорода - наблюдаются концентрации гидро-ксила выше равновесных. Имеются косвенные основания предполагать также наличие в пламени свободных радикалов С2 и СН. Сложность явления не дает возможности предложить надежную схему рассматриваемой цепной реакции. Наиболее вероятным считается, что первичное образование альдегида осуществляется каталитической, гетерогенной реакцией на поверхности стенки. В дальнейшем, при высоких температурах подобная первичная реакция может возникать и в объеме ( гомогенно) под воздействием свободных атомов и радикалов. [6]
При сжигании газового топлива уходящие газы сушил, печей и котлов обычно имеют высокую температуру и содержат значительное количество водяных паров, образующихся в продуктах горения газа в результате реакций горения углеводородов и водорода. [7]
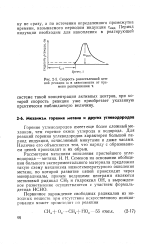 |
Скорость разветвленной цепной реакции со в зависимости от времени реагирования т. [8] |
Горение углеводородов имеет еще более сложный механизм, чем горение окиси углерода и водорода. Для реакций горения углеводородов характерен большой период индукции, исчисляемый минутами и даже часами. Наличие его объясняется тем, что наряду с образованием цепей происходит и их обрыв. [9]
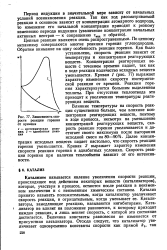 |
Зависимость скорости реакции горения от времени. [10] |
Цепные реакции являются очень распространенными. По цепному механизму совершаются многие реакции горения углеводородов Обратим внимание на одну особенность реакции горения. [11]
Ниже рассматриваются процессы неполного окисления. В этих процессах первой ступенью являются реакции горения углеводородов, к которым полностью применима теория процессов горения. Процесс проводят при недостатке кислорода, поэтому могут протекать вторичные реакции между непрореагировавшими углеводородами или продуктами их термического крекинга и двуокисью углерода и водяным паром, образовавшимися при первичном окислении или введенными вместе с кислородом. Скорость реакций горения чрезвычайно велика. Скорость вторичных реакций относительно невелика, и для обеспечения полноты их протекания процесс следует проводить при очень высоких температурах. Именно вторичные реакции лимитируют скорость процесса в целом и исходя из этого определяются размеры аппаратов, в которых проводят процесс. Роль скоростей вторичных реакций рассматривается в последующих разделах данной статьи. [12]
При применении газового топлива требуется проведение дополнительных мероприятий, обеспечивающих безопасное его использование, так как горючие газы токсичны и в определенных концентрациях в воздухе взрывоопасны. При выбросе продуктов сгорания в помещение следует особо обращать внимание на такие компоненты реакции горения углеводородов, как окись углерода, окислы азота и полициклические углеводороды - пирен и 3 4-бензпирен. Исследования, проведенные рядом организаций ( кафедрой4 теплотехники ЛИСИ, НИИ онкологии МЗ СССР, 1 - м ЛМИ, Ленгипроинжпроектом), показали, что при сжигании природного газа в газовых горелках инфракрасного излучения при температуре на излучателе 800 - 1100 С и коэффициенте избытка воздуха 1 05 полициклические углеводороды не образуются. Правильно спроектированная и нормально работающая газовая горелка инфракрасного излучения практически не должна иметь в продуктах сгорания и окиси углерода. Это подтверждается многочисленными исследованиями, проведенными разными авторами. [13]
Как видно из рис. 38, аппарат может из I кризисного состояния перейти во II кризисное состояние, а из II состояния - в III. Это можно объяснить тем, что стандартной температуре самовоспламенения паров, приводимой в справочной литературе, соответствует стехиометрическая концентрация в реакции горения углеводорода в воздухе. [14]
Из этого сопоставления следует, что в механизме горения углеводородов роль атомов Н должны выполнять радикалы R. Правда, на определенной стадии реакции, когда концентрации атомов О и радикалов ОН достаточно велики, среди активных центров реакции горения углеводородов появляются атомы Н ( например, поставляемые быстрым процессом О ОН 02 Н), которые существенным образом изменяют механизм реакции. Ввиду того, что скорость процесса R - J - 02 RO О, идущего с энергией активации, вдвое 13 превышающей энергию активации процесса Н 02 ОН О ( равную - 17 ккал), очевидно, должна быть существенно меньше скорости процесса Н - f - 02 ОН О, разветвления цепей в этом случае должны осуществляться в значительной мере этим последним процессом. [15]
Страницы: 1 2