Реакция - дегалоидирование
Cтраница 1
Реакция дегалоидирования CF2X - CF2X с помощью металла легко идет с прекрасными выходами при температурах выше 100 и может быть использована в качестве лабораторного метода получения олефина. [1]
Реакцию дегалоидирования проводят в круглодонной колбе, снабженной мешалкой, обратным холодильником и капельной воронкой. Для очистки, высушивания и фракционирования применяют аппаратуру, описанную на стр. [2]
По типу реакции дегалоидирования протекает и восстановление цианпиридинов в щелочных растворах. Особенно легко децианирование проходит в безводном этилендиамине с хлоридом лития. В этих условиях с выходами 60 - 80 % получены н-гептан, циклогептан и бицикло-гексан при восстановлении соответственно н-октилнитрила, цикло-гептилцианида и 1 1-дицианбициклогексила. [3]
Интересно, что в реакциях дегалоидирования 1 2-дихлор - 1, 2, 3, 4-тетраметилциклобутена - З [28] и 1, 2-дибромбензоцикло-бутена [5], представляющих возможные пути получения замещенных циклобутадиенов, образовались димеры строения I и II соответственно. [4]
Интересно, что в реакциях дегалоидирования 1 2-дихлор - 1, 2, 3, 4-тетраметилциклобутена - З [28] и 1, 2-дибромбензоцикло-бутена [5], представляющих возможные пути получения замещенных циклобутадиенов, образовались димеры строения 1 и II соответственно. [5]
Наиболее типичной реакцией электровосстановления с удалением заместителей является реакция дегалоидирования, которой особенно в последнее время посвящено довольно много исследований. [6]
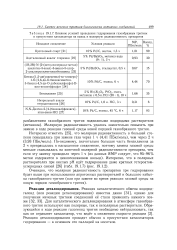 |
Влияние условий проведения гидрирования газообразным тритием в присутствии катализатора на выход и молярную радиоактивность препаратов. [7] |
Для каталитического дегалоидирования в атмосфере газообразного трития используют как полярные, так и неполярные растворители. Реакцию дегалоидирования проводят обычно в присутствии катализаторов гидрирования - в основном это палладий на носителе. [8]
Авторы показали, что здесь, как и в случае хлоракридина, принципиальным условием для направления реакции дегалоидирования в сторону восстановления, приводящего к образованию толуола, оказывается присутствие едкого натра и введение Н2 извне. В отсутствие едкого натра Н, вводимый извне, не поглощается, и реакция протекает лишь в направлении образования дибензила. [9]
Хлорметильная группа, вероятно, легче присоединяется к ядру ароматического углеводорода, чем любой другой радикал с одним атомом углерода. Реагентами являются водный формальдегид и соляная кислота в присутствии мягко действующего катализатора ( хлористый цинк), если вообще он необходим. В соединении с реакцией дегалоидирования хлорметилыгой группы это может быть общим методом превращения ароматического углеводорода в его гомологи с приращением одной или более метильной групп в ядре. В большинстве случаев можно ожидать образования смесей, но если исходный углеводород симметричного строения, то образуется один продукт. Например, толуол дает смесь трех ксилолов, в то время как n - ксилол дает исключительно псевдо-кумол. [10]
Описано несколько реакций восстановления арсиновых кислот до арсено-соединений и одна реакция восстановления до арсина ( см. табл. 92, стр. Будет ли конечным продуктом восстановления арсеносоединение или арсин, зависит, по-видимому, от концентрации кислоты. Высокая концентрация кислоты способствует образованию арсеносоединений. Интересно отметить, что при восстановлении хлорпиридинарсоновой кислоты наряду с восстановлением арсиновой кислоты протекает реакция дегалоидирования, однако восстановления пиридиновых ядер не происходит. [11]
Страницы: 1