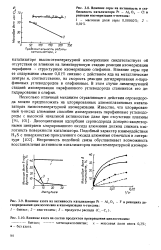
Реакция - дегидрирование - углеводород
Cтраница 1
Реакции дегидрирования углеводородов имеют много общего с гидрированием, так как они являются системой обратимых превращений. [1]
Рассмотренные выше реакции дегидрирования гексаметиле-новых углеводородов, реакции превращения пентаметиленовых углеводородов и реакции циклизации алканов являются основой современных каталитических процессов производства толуола и ароматизированных бензинов. [2]
Таким образом, реакции дегидрирования углеводородов С4 ( н-бутана и н-бутиленов) протекают эндотермически с поглощением тепла в среднем 30 ккал / моль. [3]
 |
Принципиальная схема получения ароматических растворителей. [4] |
При каталитическом риформииге протекают реакции дегидрирования шестичленных цнклановых углеводородов, дегидроизомеризацин пятичлен-ных алкилированных циклановых углеводородов и дегндроциклизации парафиновых углеводородов. [5]
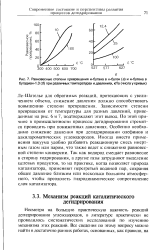 |
Равновесные степени превращения н-бутана в н-бутен ( а и н-бутена в бутадиен - ( 6 при различных температурах и давлениях, кПа ( числа у кривых. [6] |
Несмотря на большую практическую важность реакций дегидрирования углеводородов, в литературе практически не проводилось систематических исследований по изучению механизма этих реакций. [7]
В соответствии с термодинамикой для осуществления реакций дегидрирования углеводородов требуются сравнительно высокие температуры. В связи с этим катализаторы, содержащие никель, медь, платину и другие металлы 111, малопригодны для проведения этих процессов, так как при высоких температурах ( 450 - 700 С) в их присутствии углеводороды подвергаются не только дегидрированию, но и распаду. [8]
Из приведенных данных видно, что все реакции дегидрирования углеводородов сильно эндотер-мичны, и для их осуществления требуется подвод тепла. [9]
Влияние серы при ее содержании свыше 0 01 % связано с действием яда на металлические центры и, соответственно, на скорость реакции дегидрирования н-пара-финовых углеводородов в олефиновые. В этом случае лимитирующей стадией изомеризации парафинового углеводорода становится его дегидрирование в олефин. [11]
Соединения элементов побочных подгрупп I и II групп периодической системы ( в первую очередь, окиси меди и цинка) обладают заметным каталитическим эффектом в реакциях дегидрирования углеводородов и, в особенности, при дегидрировании алкильных боковых цепей. [12]
Поскольку эти элементы не имеют свободных d - ( или / -) уровней, способных участвовать в образовании связей с молекулами реагирующих веществ, они не должны давать хорошие катализаторы процессов окислительно-восстановительного типа и, в частности, реакций дегидрирования углеводородов, что и подтверждается приведенными выше фактическими данными. [13]
Судя по наличию четырех электронов на незаполненных 3 d - или 5й - орбиталях, отсутствию экранирования, легкой подвижности всех четырех электронов на d - уровнях и возможности участия их в образовании валентных связей, можно предположить, что эти окислы должны обладать высокой каталитической активностью в восстановительно-окислительных реакциях, а следовательно, и в реакциях дегидрирования углеводородов. [14]
Это позволяет проводить внутреннюю регенерацию иода и снизить отношение иод: углеводород в исходной смеси. Реакция окисления иода экзотермична, а реакции дегидрирования углеводородов эндотермичны. Одновременное их проведение в одном аппарате позволяет работать в адиабатическом режиме. Можно регенерировать иод и в отдельном аппарате; в этом случае процесс становится двухстадийным. [15]
Страницы: 1 2