Значение - потенциал - ионизация
Cтраница 2
Разница в значениях потенциалов ионизации [ / ( СН3) превышает / ( CD3) на 77 см 1 показывает, что нулевая колебательная энергия иона CHJ в основном состоянии превышает соответствующую энергию СН3 в основном состоянии и, следовательно, в таком же соотношении находятся значения сумм частот всех нормальных колебаний СН. К сожалению, значения частот колебаний молекулы СН3 как в возбужденных, так и в основном состояниях до сих пор неизвестны. [16]
Там же помещены значения потенциала ионизации V, определяющего склонность элементов к удерживанию ( или перераспределению - при сопоставлении Vt и Vi2 - двух соединяющихся в молекулу элементов) электрона. Исходя из этих параметров видно, что произойдет перераспределение электронного облака преимущественно в сторону кислорода вследствие меньшей величины V, ( Si) и более низко расположенных свободных электронных орбит. [17]
Согласно этой теореме, значение потенциала ионизации приравнивают к значению энергии соответствующей занятой МО, взятому с обратным знаком. Значение электронного сродства приравнивают к значению энергии соответствующей свободной МО, взятому с обратным знаком. [18]
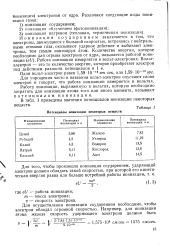 |
Потенциалы ионизации некоторых веществ. [19] |
В табл. 1 приведены значения потенциалов ионизации некоторых веществ. [20]
 |
Потенциалы ионизации химических элементов ( в эВ. [21] |
В табл. 4 приведены значения потенциалов ионизации для элементов первого и второго периодов. [22]
В табл. 7 приведены значения потенциала ионизации некоторых элементов. [23]
На рис. 1.7 сравниваются значения потенциалов ионизации и электронного сродства этилена, бутадиена и бензола. [24]
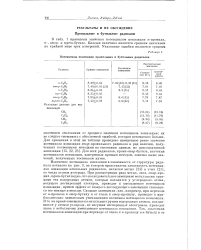 |
Потенциалы ионизации пропидьных и бутильных радикалов. [25] |
В табл. 1 приведены значения потенциалов ионизации к-пропилаг к -, втор - и тгерето-бутила. Каждая величина является средним значением по крайней мере трех измерений. [26]
В табл. 13 приведены значения потенциалов ионизации ряда элементов. Наблюдается резкое различие потенциалов ионизации у электронов различных энергетических уровней элементов. Различные энергетические уровни в таблице отделены жирной чертой. [27]
В табл. 2 приведены значения потенциалов ионизации галогенозаме-щенных метильных радикалов. [28]
Приведенные в данном параграфе значения потенциалов ионизации и СЭ широко используются в структурной химии как для квантовохимиче-ских расчетов, так и для полуэмпирических оценок. С этими применениями энергетических характеристик атомов мы еще встретимся в дальнейшем изложении, а пока заметим, что в большинстве случаев исследователи пользуются первыми потенциалами ионизации и СЭ. Если СЭ ко 2-му и тем более к 3-му е - не соответствует никакой реальности, так как в природе не существует ионов Аг - и А3 -, то использование первых потенциалов ионизации, по существу, основано на уравнении Глокклера - Лисицына, которое функционально связывает остальные потенциалы с первым потенциалом ионизации атома. [29]
Атомы элементов отличаются также значениями потенциалов ионизации Ut. [30]
Страницы: 1 2 3 4