Каталитическая гетерогенная реакция
Cтраница 1
Каталитические гетерогенные реакции в газовой фазе хорошо изучены для хлорирования главным образом низших углеводородов. В качестве катализаторов в этом случае применяют активированный уголь, хлорную медь, нанесенную на активированный уголь, пемзу или силикагель. [1]
Каталитической гетерогенной реакцией называют гетерогенную реакцию, при которой продукты реакции не содержат элементов, входящих в состав материала поверхности. [2]
Механизм каталитических гетерогенных реакций очень сложен и зависит от природы реакции. Все каталитические гетерогенные реакции включают в себя стадии адсорбции и десорбции. За счет энергии адсорбционного взаимодействия с поверхностными атомами катализатора ослабляются, а иногда и разрываются, химические связи реагирующих частиц. [3]
Круг каталитических гетерогенных реакций чрезвычайно обширен и разнообразен, причем столь же разнообразными являются и применяемые катализаторы. [4]
Реакция оксиэтилирования является каталитической гетерогенной реакцией, протекающей в две стадии: 1-я - диффузия и растворение газообразной окиси этилена в расплавленном оксиэтилируембм соединении, 2-я - сам акт присоединения окиси этилена к этому соединению. [5]
Адсорбция представляет собой необходимую промежуточную стадию каталитических гетерогенных реакций. [6]
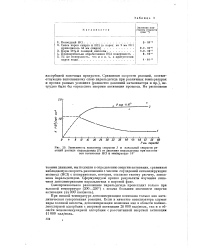 |
Зависимость константы скорости 1 и начальной скорости реакций распада паральдегида ( 2 от давления паральдегида при постоянном количестве НС1 и температуре 16. [7] |
При низкой температуре деполимеризация возможна только как каталитическая гетерогенная реакция. Если в качестве катализатора служат пары соляной кислоты, деполимеризация возможна как в области полимолекулярной адсорбции с энергией активации 26 000 кал / моль, так и в области мономолекулярной адсорбции с рассчитанной энергией активации 11 000 кал / моль. [8]
Принимая во внимание это условие, на первый взгляд может показаться удивительным, что каталитические гетерогенные реакции часто протекают значительно быстрее, чем реакции, проходящие целиком в газовой фазе. [9]
Непрерывный теплообмен возможен также при наличии в твердом теле Источника ( Стока) теплоты - скажем, при проведении каталитической гетерогенной реакции с тепловым эффектом: теплота реакции воспринимается здесь сплошной средой при постоянных локальных температурах твердого материала и среды. Во втором случае ( периодические и полунепрерывные процессы) теплообмен является нестационарным: температура твердых тел ( крупные элементы, зерна, мелкие частицы) изменяется во времени, в уравнениях теплового баланса появляется составляющая Накопление; среда обычно имеет постоянную входную температуру, температура среды на выходе из рабочей зоны может изменяться во времени. Заметим, что при осуществлении стационарных ( применительно к рабочей зоне теплообменника) процессов отдельные акты теплопереноса ( по отношению к индивидуальному зерну, например) чаще всего нестационарны. [10]
Механизм каталитических гетерогенных реакций очень сложен и зависит от природы реакции. Все каталитические гетерогенные реакции включают в себя стадии адсорбции и десорбции. За счет энергии адсорбционного взаимодействия с поверхностными атомами катализатора ослабляются, а иногда и разрываются, химические связи реагирующих частиц. [11]
В гомогенной среде в отсутствие катализатора реакция протекает с достаточной скоростью лишь при 800 - 1000 С. Промышленное значение имеет каталитическая гетерогенная реакция, позволяющая вести процесс на высоких скоростях газового потока и с удовлетворительной степенью конверсии метана уже при 550 - 700 С. [12]
Тем не менее, в известной монографии Глэсстона, Лейдлера, Эйринга [8] именно этот тип реакции авто ы используют ( см. стр. Разделив значение / с, определенное из уравнения типа ( 6), на значение 7i0 для гомогенной газофазной реакции, авторы получают очень низкие значения отношения л0 ет / / с, гом - 10 - 12 и после этого удивляются, что каталитические гетерогенные реакции часто протекают значительно быстрее, чем реакции, проходящие целиком в газовой фазе. В действительности, ничего удивительного ( в этом смысле) в гетерогенном катализе нет и незачем для объяснения несоответствия привлекать, как это делают авторы [8], низкую энергию активации гетерогенно-каталитических реакций. Все дело в том, что сопоставляются несопоставимые реакции. [13]
Гомогеннокаталитические реакции составляют лишь небольшую долю каталитических реакций, используемых при получении промежуточных продуктов. Значительно большую роль при синтезе промежуточных продуктов играет гетерогенный катализ, особенно катализ в паровой фазе. Круг каталитических гетерогенных реакций чрезвычайно обширен и разнообразен, причем столь же разнообразны применяемые катализаторы. Так, металлы платиновой группы, медь и окислы железа, никеля, хрома, молибдена и др. служат катализа торами в процессах гидрирования молекулярным водородом; окислы ванадия; молибдена, вольфрама, железа, марганца, меди, серебра, кобальта, никеля используются в качестве катализаторов различных реакций окисления; для реакций дегидратации применяются окислы алюминия, кремния, тория, хрома и вольфрама. [14]
Спектроскопическими исследованиями было показано, что, так же как и в случае окисления Н2 и СО, в зоне реакции горения углеводорода - наблюдаются концентрации гидро-ксила выше равновесных. Имеются косвенные основания предполагать также наличие в пламени свободных радикалов С2 и СН. Сложность явления не дает возможности предложить надежную схему рассматриваемой цепной реакции. Наиболее вероятным считается, что первичное образование альдегида осуществляется каталитической, гетерогенной реакцией на поверхности стенки. В дальнейшем, при высоких температурах подобная первичная реакция может возникать и в объеме ( гомогенно) под воздействием свободных атомов и радикалов. [15]
Страницы: 1