Хемилюминесцентная реакция
Cтраница 1
Хемилюминесцентная реакция на перекись водорода была использована с большим успехом в текстильном деле [4]: ткани из ацетатного шелка, на которых наведен мат двуокисью титана, оказывались непрочными, причина этого оставалась непонятной; реакция с люминолом позволила обнаружить образование перекиси водорода, ею и обусловливается разрушение волокна. Текстильщики, поняв причину порчи шелка, сумели ее устранить. [1]
Хемилюминесцентные реакции занимают особое место в кинетических методах анализа. С помощью люминола возможно косвенное ( по ингибиторному действию катионов, способных связывать перекись водорода или дезактивировать перекисные радикалы) определение ванадия и циркония ( см. настоящий сборник, стр. Хе-милюминесценция люцигенина использована для определения следов осмия и кобальта. [2]
Сначала хемилюминесцентные реакции изучали визуально. Затем для определения суммы света, выделяющегося при хемилюминесцентной реакции и для практического применения в анализе был предложен фотографический метод. [3]
Хемилюминесцентная реакция образования формальдегида, по-видимому, может быть использована в целях исследования реакций радикалов СН30 и ОН с различными молекулами. Эти реакции могут быть изучены в струевой установке по распределению свечения в трубе в отсутствие и в присутствии вещества, реагирующего с одним из радикалов. [4]
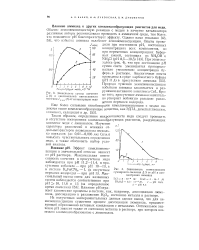 |
Зависимость суммы свечения 2 ( 1 и. максимальной интенсивности свечения / М1КС ( 2 от концентрации меди.| Зависимость интенсивности суммарного свечения Д S от рН и концентрации аммиака. [5] |
Обычно хемилюминесцентную реакцию с медью в качестве катализатора различные авторы рекомендовали проводить в аммиачной среде, тем более, что повышение рН благоприятствует эффекту. Однако нами показано [43, 53], что избыток аммиака ослабляет хемилюминесценцию. [6]
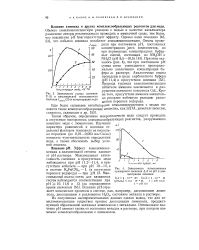 |
Зависимость суммы свечения 2 ( / и максимальной интенсивности свечения / макс ( 2 от концентрации меди.| Зависимость интенсивности суммарного свечения Д S от рН и концентрации аммиака. [7] |
Обычно хемилюминесцентную реакцию с медью в качестве катализатора различные авторы рекомендовали проводить в аммиачной среде, тем более, что повышение рН благоприятствует эффекту. Однако нами показано [43, 53], что избыток аммиака ослабляет хемилюминесценщда. [8]
Некоторые хемилюминесцентные реакции, несмотря на малый квантовый выход хемилюминесценции, применяют для различных целей. [9]
Примерами хемилюминесцентных реакций с малыми квантовыми выходами могут служить реакции окисления молекулярным кислородом углеводородов, алифатических кислот и альдегидов в жидкой и газовой фазах. [10]
Механизм хемилюминесцентных реакций крайне сложен и до конца не выяснен. Большое значение в хемилюминесценции имеют процессы комплексообра-зования, каталитического разложения пероксида водорода, радикальные процессы. [11]
Изучен химизм хемилюминесцентных реакций в системах люминол - металл ( медь, кобальт) - перекись водорода, а также в присутствии ряда органических и неорганических ингибиторов. Изучено влияние отдельных компонентов реакции и установлены оптимальные условия ведения реакций в названных системах. [12]
Изучен химизм хемилюминесцентных реакций в системах люминол - металл ( медь, кобальт) - перекись водорода, а также в присутствии ряда органических и неорганических ингибиторов. Изучено влияние отдельных компонентов реакции и установлены оптимальные условия ведения реакций в названных системах. [13]
Основоположником применения хемилюминесцентных реакций в анализе является А. К. Бабко и его ученики. [14]
В аналитической практике хемилюминесцентные реакции используют: 1) для установления точки эквивалентности при титровании мутных или окрашенных растворов ( применение хемилюминесцентных индикаторов в методах нейтрализации, окисления - восстановления, комплексообразования); 2) для определения основных компонентов хемилюминисцентных реакций ( хемилюминесцентного реактива, окислителя или восстановителя), 3) для определения микроколичеств ионов металлов, которые являются катализаторами или ингибиторами хемилюминесцентных реакций; 4) для определения органических веществ, которые являются ингибиторами хемилюминесцентных реакций, по их окислению. [15]
Страницы: 1 2 3 4