Изолированная реакция
Cтраница 1
Изолированная реакция, для которой А и 0, невозможна. Такое суммирование отвечает термодинамическому сопряжению реакций. Благодаря термодинамическому сопряжению в открытых системах протекают процессы, не реализуемые в изолированных системах. [1]
Изолированные реакции - реакции, в ходе которых образуется продукт только одного типа. [2]
Изолированную реакцию, или рефлекс, можно получить в лаборатории на препарате лягушки, но никак не на живом человеке. У живого человека рефлексы находятся в постоянной и нерасторжимой связи друг с другом, и при этом оказывается, что в зависимости от характера и структуры каждой группы меняется и характер входящего в ее состав рефлекса. Таким образом, рефлекс есть величина не постоянная, раз навсегда данная, но переменная от раза к разу и не самостоятельная, а зависимая от общего характера поведения в данную минуту. [3]
Тем не менее метод изолированных реакций широко используется в химии, и во многих случаях он оказывается достаточно точным для приближенного ( или даже весьма точного) описания свойств системы. Самая простая картина наблюдается в том случае, когда химическое превращение можно описать с помощью одного уравнения баланса масс - привычного стехиометрического уравнения химической реакции. Для этого случая термодинамическая теория развита наиболее полно, и ее широко используют в химии. Важно только иметь в виду, что подобное описание является первым приближением, а не закопченной теорией химических равновесий. [4]
Предметом наших рассмотрений мы решили сделать простейший случай изолированной реакции, которая может быть разбита на элементарные стадии. [5]
Иными словами, в наше рассмотрение мы включаем окружение изолированной реакции для того, чтобы описать так называемую парциальную реакцию всей системы. Эти результаты могут быть обобщены следующим образом: для получения любого высказывания о рассматриваемой реакции нам необходимо выбрать булеву подрешетку соответствующей ортомодулярной решетки, нарушив целостный характер реакции. [7]
Относительная реакционная способность иодбензола и бром-бензола по отношению к фосфоранионным нуклеофилам для изолированных реакций сильно отличается от относительной реакционной способности, определенной в экспериментах по конкурентному реагированию с одним и тем же нуклеофилом. Такой эффект вовлечения широко распространен для реакций, протекающих по механизму SRN. [8]
На основе этого закона устанавливаются определенные, так называемые стехиометрические соотношения, справедливые не только для одной изолированной реакции, но и при совместном протекании группы реакций как последовательных, так и параллельных. Разрабатываемый Дерманом метод стехиометрического анализа [53, 54] сложного химического процесса, состоящего из совокупности реакций, роль и взаимодействие которых недостаточно выяснены, дает возможность проверки тех или иных гипотез о протекании данного процесса и раскрытия связи между отдельными реакциями. [9]
Для установления степени соответствия законов в гомогенной и гетерогенной кинетике мы предложили следующую общую идею: Скорость любой изолированной реакции является произведением эффективной удельной скорости на величину эффективной реакционной поверхности. Это правило хорошо проверено и основывается на законе заполнения среды продуктами реакции при условии, что зона реакции единственна и однородна. [10]
Константы А и ЕА уравнения Аррениуса ( 1) имеют ясный физический смысл, только когда относятся к простым изолированным реакциям. Поэтому одной из наиболее трудных и важных задач химической кинетики является выделение отдельных стадий сложных механизмов, по которым обычно протекают реакции в растворах. Ниже рассмотрено несколько простых примеров. [11]
Эта задача не всегда может быть разрешена при лабораторном изучении кинетики сложных реакций, так как трудно создать условия, при которых можно исследовать кинетику одной изолированной реакции, исключив остальные, если приходится иметь дело с объектами, химические превращения которых достаточно сложны. [12]
Для простых изолированных систем степень диссоциации находится легко через константу равновесия. Рассмотрим две простые изолированные реакции. [13]
В следующих трех главах рассматриваются поведение и характер действия агрохимикатов в трех сферах окружающей среды - почве, воде и воздухе. Однако это не означает, что речь идет об изолированных реакциях. Важная особенность агрохимикатов по сравнению с другими химикатами и отходами производства, попадающими в окружающую среду, заключается исключительно в том, что при правильном ведении сельского хозяйства протекают целенаправленные реакции, за ходом и последствиями которых можно следить. [14]
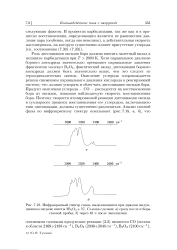 |
Инфракрасный спектр газов, выделяющихся при прямом индукционном нагреве шихты 2В2Оз 7С. Съемка сделана. а сразу после отбора. [15] |
Страницы: 1 2
