Изотермическая реакция
Cтраница 3
Для расчета следующего периода - изотермической реакции - требуется только уравнение материального баланса со значением k при 95 С. [31]
При низких давлениях в условиях изотермической реакции наблюдаемое ио-гвышение давления определяется только увеличением числа молекул. [32]
По мере исчерпания реагирующих веществ изотермической реакции скорость ее будет непрерывно падать. [33]
 |
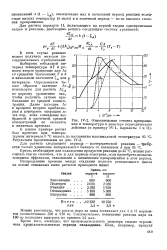
Кинетические кривые окисления этана ( по Садовяинову. [34] |
При низких давлениях в условиях изотермической реакции наблюдаемое повышение давления определяется только увеличением числа молекул. [35]
 |
Относительная степень превращения и температура в реакторе периодического действия ( к примеру IV-1, варианты I и II. [36] |
Для расчета следующего периода - изотермической реакции - требуется только уравнение материального баланса со значением k при 95 С. [37]
Ранее рассмотрен расчет равновесного состава для изотермических реакций. В реальных технических процессах, например, платформинге, гидрокрекинге, при окислении топлива в реактивном двигателе и др., реакции протекают в условиях, близких к адиабатическим. Для адиабатической реакции расчет равновесного состава по величине константы равновесия осложнен тем, что нужно предварительно установить температуру реакционной смеси на выходе из аппарата ( или в конце процесса), но, в свою очередь, эта температура определяется возможной глубиной превращения. Таким образом, при расчете адиабатических реакций приходится пользоваться методом подбора, чтобы обеспечить соответствие выходных температур и равновесного состава. Рассматриваемая ниже схема расчета адиабатической реакции справедлива для любых условий ее осуществления в проточных или статических аппаратах. [38]
Ниже для простоты изложения рассматривается случай изотермических реакций ( для которых все kq const) в статических условиях; обобщение полученных ниже результатов на неизотермические реакции в потоке не представляет принципиальных затруднений. [39]
Для того чтобы изучить класс механизмов гетероген-но-каталитических изотермических реакций в ППР, Мортон и Гудман [132] провели анализ устойчивости и бифуркаций простых моделей. Было найдено, что уравнения баланса массы согласуются с решениями типа предельного цикла. Показано, что при определенных значениях параметров модель элементарной стадии со стехиометрией окисления СО обладает колебательным поведением. [40]
Вначале, как и в случае сложной изотермической реакции, должны быть выявлены независимые реакции. [41]
Такой подход дает точные результаты для изотермической реакции нулевого порядка. Однако при анализе реакций высших порядков, а также реакций, сопровождающихся сильной адсорбцией продуктов, неизотермических систем и других сложных случаев расхождения становятся значительными. [42]
Упрощенная физическая задача включает в себя изотермическую реакцию А - - В, которая катализируется в грануле длиной две единицы. [43]
В периодически действующем аппарате с мешалкой протекает изотермическая реакция. [44]
Тепловой взрыв возникает уже в начальной стадии предвзрывной изотермической реакции после израсходования незначительной части исходных продуктов. Скорость этой реакции линейно зависит от концентрации активного промежуточного компонента х, а поэтому и от количества прореагировавшего вещества. [45]
Страницы: 1 2 3 4