Химическая реакция - вещество
Cтраница 1
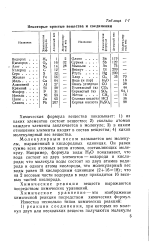 |
Некоторые простые вещества и соединения. [1] |
Химические реакции веществ выражаются посредством химических уравнений. [2]
Химические реакции веществ в коллоидно-дисперсном состоянии ускоряются и каталитическое действие усиливается. [3]
Большинство химических реакций веществ, имеющих практическое значение, являются сложными. [4]
Вступающие в химическую реакцию вещества имеют, таким образом, определенный запас внутренней энергии, как и вещества, получающиеся в результате реакции. Этот избыток энергии ( энергетический эффект) частично идет на нагревание продуктов реакции, частично лее излучается в виде квантов тепловой энергии. При эндотермической реакции, наоборот, внутренняя энергия получающихся веществ больше, чем вступающих в реакцию веществ, и в количестве, равном этой разности, необходим ( для течения реакции) приток энергии извне. [5]
Однако при химических реакциях вещества расходуются и образуются в мольных соотношениях, и поэтому для материальных расчетов более удобны их мольные количества nit выраженные в моль или кмоль. [6]
При протекании некоторых химических реакций вещества, участвующие в них, излучают свет; это явление называется хемилюминесценцией. Сюда относится свечение желтого фосфора, который медленно окисляется на воздухе. Соединение этого элемента с кислородом, как правило, сопровождается довольно интенсивным испусканием света. Существуют и другие вещества, которые, вступая в реакцию соединения с кислородом, излучают яркий свет самых разнообразных окрасок. [7]
Влияние на скорость химической реакции веществ, не являющихся ни реагентами, ни продуктами реакции, называют катализом. [8]
Объемы реагирующих в процессе химической реакции веществ вычисляют исходя из молярных количеств этих веществ и молярных объемов. [9]
Известно, что при химических реакциях вещества взаимодействуют между собою в количествах, равных или кратных грамм-эквивалентам этих веществ. [10]
Переход химической энергии в тепловую происходит при химической реакции веществ. [11]
С другой стороны, известно, что в химической реакции вещества реагируют между собой в эквивалентных количествах. Таким образом, при титровании число миллиграмм-эквивалентов реактива, прибавленного в виде рабочего раствора, в точке эквивалентности равно числу миллиграмм-эквивалентов определяемого вещества. [12]
Другие принципы измерений используют фотоэлектрические детекторы для определения химической реакции тестируемого вещества, проявляющейся с избирательно действующими реактивами. [13]
Вторая задача эксперимента и заключается в том, чтобы показать химические реакции вещества в возможно наглядной форме. Вне зависимости от того, проводится ли эксперимент в виде иллюстрации к сказанному учителем или, отправляясь от опыта, учащиеся делают выводы о свойствах вещества, эксперимент должен обеспечить живое созерцание действительности. [14]
В соответствии с законом эквивалентов число грамм-эквивалентов всех участвующих в химической реакции веществ должно быть одинаково. [15]
Страницы: 1 2 3 4