Первичная химическая реакция
Cтраница 1
Первичные химические реакции между топливом и окислителем происходят в зоне раскаленного кокса. [1]
Вторичными называются реакции, происходящие между продуктами первичной химической реакции и газифицирующими реагентами или твердым углеродом кокса. [2]
Эти реакции происходят в реакционном центре и являются первичными химическими реакциями фотосинтеза. Таким образом, индуцированные светом перемещения электрона в реакционном центре в конечном итоге приводят к переносу его на вторичный акцептор с отрицательным потенциалом. [3]
Второй закон фотохимии сформулировали Штарк и Эйнштейн: каждая молекула, участвующая в первичной химической реакции, идущей под действием света, поглощает один квант энергии ( один фотон), который и вызывает реакцию. [4]
Теплота взрывчатого превращения, измеряемая в калориметре, так называемая калориметрическая теплота взрыва, является интегральной характеристикой ВВ и представляет собой суммарный тепловой эффект первичных химических реакций, протекающих во фронте детонационной волны ( ДВ), и вторичных равновесных реакций, происходящих при адиабатическом расширении ПВ после завершения детонации. По этому закону суммарный тепловой эффект некоторой последовательности химических реакций не зависит от пути превращения исходных веществ в конечные продукты, а определяется только начальным и конечным состоянием системы. Общий тепловой эффект равен алгебраической сумме тепловой эффектов промежуточных реакций. [5]
Первичными называются реакции, происходящие между углеродом кокса и газифицирующими реагентами. Вторичными называются реакции, происходящие между продуктами первичной химической реакции и газифицирующими реагентами или твердым углеродом кокса. [6]
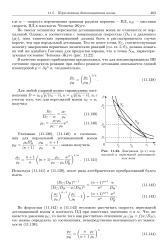 |
Диаграмма ( p - v нормальной и пересжатой детонационных волн. [7] |
По своему механизму пересжатая детонационная волна не отличается от нормальной. Тем не менее точка TVc, соответствующая моменту завершения первичных химических реакций ( см. гл. [8]
Действие света на раствор смеси флуоресцирующего красителя и восстановителя может вызвать выцветание красителя или обратимое или необратимое окисление восстановителя. Для объяснения первичных химических реакций был предложен механизм переноса электронов. Фотохимическая активность некоторых сортов окиси цинка была связана с тем фактом, что окись цинка не обладает флуоресценцией в видимом свете при комнатной температуре после облучения ультрафиолетовым светом. Было высказано предположение, что богатая энергией часть солнечной радиации является источником фотохимической энергии, в то время как в тех сортах окиси цинка, которые обладают сильной желтой флуоресценцией, энергия рассеивается в виде излучения с более низким уровнем 132 энергии. Между флуоресценцией и фотосенсибилизацией существует сложная зависимость; ш поэтому интересно изучить флуоресценцию активных кубовых красителей в присутствии целлюлозы. [9]
Зависимость между логарифмом выживания и дозой характеризуется у диметилмилерана четким порогом, в то время как у азотистого иприта зависимость была почти линейной. По внешнему виду клетки различались в зависимости от вводимого вещества, из чего был сделан вывод о разнице в первичных химических реакциях, оказывающих действие на рост, поскольку алкилировались различные участки. [10]
Даже если абстрагироваться от возможных эффектов подобного рода, все равно надо признать, что механизм химического зародышеобразования довольно сложен. По-видимому, нелегко предвидеть ( даже качественно) то влияние, которое могут оказать на Зародышеобразование различные экспериментальные параметры. Рассмотрим, например, влияние повышения температуры. Протекание первичных химических реакций, предшествующих зародышеобразованию, при повышении температуры должно облегчаться. Но влияние температуры на процесс ассоциации промежуточных частиц в зародыш значительно сложнее. [11]
Он предполагает миграцию зарядов по зоне проводимости или валентной зоне ( в последней возникают светоиндуцированные вакансии) к центрам захвата - химическим акцепторам или донорам электронов. При экситонной миграции энергии в пигментной матрице нейтральный экситон может мигрировать к реакционному центру, где и происходит его диссоциация на два противоположно заряженных носителя. В этом случае носители заряда раздельно мигрируют в матрице: электронная вакансия ( р) захватывается в активном центре, приводя к образованию катион-радикала хлорофилла ( бак-териохлорофилла), а электрон ( е) - первичным акцептором, который может быть локализован вдали от активного центра. Центры захвата носителей заряда в пигментной матрице, обладающие низкой потенциальной энергией, разделены в пространстве в результате миграции зарядов по зоне проводимости или валентной зоне. В них инициируются первичные химические реакции фотосинтеза. [12]
Фотохимическими называются реакции, происходящие под действием света. Химическое действие света известно более 100 лет. Установлено, что большинство фотохимических реакций - многостадийные процессы, которые начинаются с поглощения фотона молекулой и образуется возбужденное электронно-колебательное состояние. Последнее крайне неустойчиво и за время, меньшее 10 - с, излучая энергию, переходит в другое, менее возбужденное состояние. Возбужденные молекулы вступают в первичные химические реакции после перехода в менее возбужденное состояние. Продукты первичных фотохимических реакций - радикалы, ионы - быстро вступают во вторичные реакции, приводящие к образованию конечных продуктов. [13]
Фотохимическими называются реакции, происходящие под дей - ствием света. Химическое действие света известно более 100 лет. Установлено, что большинство фотохимических реакций - многостадийные процессы, которые начинаются с поглощения фотона молекулой и образуется возбужденное электронно-колебательное состояние. Последнее крайне неустойчиво и за время, меньшее 10 - с, излучая энергию, переходит в другое, менее воз - бужденное состояние. Возбужденные молекулы вступают в первичные химические реакции после перехода в менее возбужденное состояние. Продукты первичных фотохимических реакций - радикалы, ионы - быстро вступают во вторичные реакции, приводящие к образованию конечных продуктов. [14]
Страницы: 1