Значение - скорость - горение
Cтраница 1
 |
Зависимости скорости горения от давления. [1] |
Значения скоростей горения, получаемые на модельных РДТТ, часто приходится увеличивать на 1 - 3 %, чтобы обеспечить соответствие со скоростями горения в полномасштабных двигателях. Наибольшие корректировки требуются для двигателей с корпусом из стекловолокна, в которых вследствие совместного расширения ТРТ и корпуса при повышении давления изменяется толщина свода горения заряда. На рис. 55 показаны различные формы зависимости скорости горения ТРТ от давления в камере. Прямая линия соответствует обычному степенному закону г аркп. [2]
 |
Скорость горения стехиометрических смесей ацетилена и окислов азота. [3] |
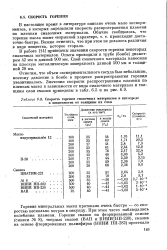
Значения скоростей горения при пониженных давлениях даны в табл. VII.8. Данные [16] о влиянии различных разбавителей ia скорость распространения пламени ( которая зависит также от конструкции чрелки) для стехиометрической смеси С2Н2 2 5 О2 представлены, кроме того, ) табл, VIII. [4]
 |
Скорость горения смазочных материалов в кислороде в зависимости от толщины их слоя. [5] |
В работе [14] приведены значения скорости горения некоторых смазочных материалов. [6]
Следует отметить, что значения скорости горения различных смазочных материалов значительно отличаются одно от другого. [7]
 |
Скорость горения. [8] |
При сравнении найденных значений со значениями скорости горения в чистом кислороде видно, что снижение концентрации кислорода со 100 до 70 объемн. [9]
Возможно поэтому, что полученные нами значения скоростей горения при высоких давлениях для образцов малой плотности завышены. [10]
Величина давления, при котором горение переходит на пульсирующий режим, и значения скорости горения различны для разных ВВ. Так, для метилнитрата это происходит при 1 75 ат, причем скорость горения составляет около 0 26 г / см2 сек, для нитрогликоля пульсирующее горение наступает при 17 ат и скорости горения 0 79 г / см. сек, для нитроглицерина ( t 98 С) - при 0 4 ат и скорости горения 0 12 г / см2 сек. [11]
Изученные нитроэфиры в отношении скоростей термического распада-практически равнозначны ( энергия активации равна 35 - 39 ккал / молъ для нитрогликоля, 42 5 ккал / молъ для диэтиленгликольдинитрата [69] и 38 ккал / молъ для этилнитрата), однако они сильно различаются по скоростям горения. Если значения скоростей горения для этих нитроэфиров нанести на один график, как это сделано в книге Андреева [53], то быстрее всех горит нитрогликоль, за ним следует диэтиленгликольдинитрат и этилнитрат, что находится в соответствии с их температурами горения. [12]
Ввиду большого разброса значений скоростей горения не проведена кривая на графике рис. 22, можно лишь констатировать, что в среднем скорость горения мало меняется с давлением и в интервале 10 - 100 ат составляет 2 - 3 г / см2 - сек. Заметим, что при горении тетрила и пикриновой кислоты такая скорость достигается лишь при давлениях порядка 400 - 500 ат. [13]
Из табл. 10 - 2 видно, что массовая скорость горения, отнесенная к фронту пламени для одного и того же горючего, не зависит от величины и формы зеркала испарения и является постоянной величиной. Некоторые отклонения в значениях скорости горения, отнесенной к фронту пламени, объясняются трудностями определения поверхности факела. [14]
Один из путей стабилизации горения жидких ВВ заключается в увеличении их вязкости. Из рис. 9 видно, что значения скоростей горения для дины с 3 % коллоксилина хорошо ложатся на пунктирную кривую 3, являющуюся продолжением кривой для переохлажденной дины, горящей в ламинарном режиме. [15]
Страницы: 1 2