Значение - температура - затвердевание
Cтраница 1
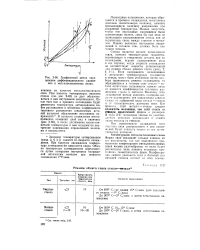 |
Графический метод определения дифференциального удлинения в металлостеклянных спаях. [1] |
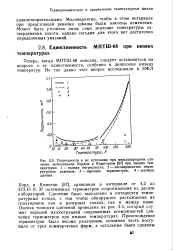
Значение температуры затвердевания ( разд. При быстром охлаждении температура затвердевания сдвигается вверх. [2]
Совокупность приведенных в таблице значений температур затвердевания и кипения, а также удельных весов и показателей преломления позволяет ( Квалифицировать полученные спирты как содержащие 90 - 95 % основного вещества. [3]
Для исключения загрязнений поверхностей нагрева, расположенных за топкой, важно охладить в топке газы до температуры ниже значения температуры затвердевания золы, наступающего после прохождения ею области высоких температур. Обычно величина этой температуры ниже / 2 на 50 - 100 С. При горении топлива в топке в зоне высоких температур происходит частичное или полное расплавление золы. Некоторая часть ее образует летучую золу ( унос), которая уходит с топочными газами из топки. Оставшаяся зола, частично разлагаясь, превращается в сплавленную или спекающуюся массу, называемую шлаком, который затем в жидком или гранулированном состоянии удаляется из нижней части топки. [4]
Вследствие этого температура плавления шлака отличается от температуры плавления золы ta - Для борьбы с загрязнением поверхностей топочной камеры особенно важно знать значение температуры затвердевания золы, наступающего после прохождения ею зоны высоких температур - оно обычно ниже tz примерно на 50 С. [5]
Полученные нами результаты говорят о том, что если точке затвердевания серебра приписать более высокое значение, то это приведет к лучшему совпадению шкалы термометра сопротивления со шкалой термопары, и, следовательно, наилучшее в этом отношении значение температуры затвердевания серебра равно 960 9 С. [6]
Следует заметить, что значение температуры затвердевания кислоты в ампулах отличалось от значений температуры тройной точки бензойной кислоты и температуры затвердевания в сухом воздухе при давлении 1 атм, так как в ампуле создавались условия, промежуточные между двумя указанными определенными состояниями. [7]
Маловероятно, чтобы в этом интервале при предстоящей ревизии шкалы были внесены изменения. Может быть уточнено лишь само значение температуры затвердевания золота, однако сегодня для этого нет достаточно определенных указаний. [9]
Платиновая термопара применяется в интервале от 660 до 1063 С и градуируется в точках плавления золота, серебра ( 960 5 С) и сурьмы ( 630 5 С) для того, чтобы найти постоянные квадратного уравнения. Точка сурьмы не является первичной реперной точкой и значение температуры затвердевания каждого используемого образца определяется термометром сопротивления, что обеспечивает непрерывность шкалы в этой точке. К сожалению, однако ( по некоторым причинам, которые теперь не ясны), точка деления шкалы была установлена при 660 С. Это привело к курьезному результату ( отмеченному Бюро стандартов во время дискуссии о пересмотре шкалы в 1939 г.), заключавшемуся в том, что точка затвердевания чистого алюминия не могла быть измерена в Международной шкале температур. Если же производить измерения при помощи термопары, то значение этой точки оказывается ниже 660 С, и, следовательно, должно измеряться термометром сопротивления. По оценке Бюро стандартов расхождение между двумя частями шкалы составляет около 0 15 С. Для того чтобы исключить это расхождение, заседание Консультативного комитета по термометрии в 1939 г. предложило в дальнейшем разделять шкалу при 630 5 С - температуре, примерно соответствующей значению точки сурьмы. Однако начавшаяся война помешала созвать Конференцию по мерам и весам, и это предложение не было утверждено. [10]
Как уже было указано в § 1, для применения термодинамики необходимо выражать температуру по шкале, предложенной Кельвином. Для перехода от шкалы газового термометра к шкале Кельвина нужно знать значение коэффициента ал. Ввиду первостепенного значения этого вопроса для термометрии мы начнем, по примеру Даниеля Вертело [ 31, с рассмотрения значения, которое следует приписать этой физической константе, или, другими словами, значению температуры затвердевания воды по шкале Кельвина. [11]
По ходу данной работы не было обнаружено заметного необратимого разложения бензойной кислоты, если она нагревалась до температур не выше 150 С. Доказательство этому будет приведено ниже. Эту реакцию следует контролировать, так как недопустимо изменение чистоты или прогрессивное возрастание загрязнений, вызывающее соответствующие изменения в температуре затвердевания. По исследованию процесса разложения было поставлено много экспериментов. Если кислота находится в запаянной ампуле, то образующаяся одновременно с ангидридом вода не может уходить из сферы реакции, и реакция поэтому может протекать только до тех пор, пока не установится равновесие. Предполагалось, что для наблюдения воспроизводимой точки плавления кислоту необходимо привести в некоторое состояние равновесия с продуктами ее разложения. Сообразно этому предположению, четыре ампулы поддерживались при температуре выше температуры затвердевания ( за исключением короткого периода, в течение которого производились измерения температуры затвердевания) до тех пор, пока не достигалось равновесие; состояние равновесия характеризовалось постоянством температуры затвердевания кислоты в ампулах. Температура печи примерно на 10 С превышала температуру затвердевания кислоты. Следует заметить, что для достижения равновесия между бензойным ангидридом и водой требуется не менее 10 дней. Небольшой разброс в значениях температуры затвердевания за период до 8 недель связан с растворением в кислоте небольшого количества ангидрида и воды ( около 0 015 мол. Небольшое различие значений температур затвердевания для отдельных ампул в вакууме объясняется, вероятно, различием исходного содержания воды или ангидрида, так как при наполнении ампул и сушке кислоты количество обеих компонент строго не контролировалось. [12]
После этого температура повышалась примерно на 10 С сверх температуры затвердевания, и продувался воздух, насыщенный водой при - 25 С. Кислота переохлаждалась примерно наО 5 С. При внезапном образовании кристаллов температура подымалась до температуры равновесия ( в пределах нескольких тысячных градуса) в течение 2 мин. После того как затвердевало около 5 % кислоты, температуру масляной ванны быстро повышали до температуры затвердевания кислоты и поддерживали постоянной в пределах 0 01 С. Температура затвердевания при этих условиях была равна 122 369д С. Потом кислоту перемешивали воздухом, который просушивали над пятиокисью фосфора, до тех пер, пока температура не принимала постоянное значение, равное 122 3742 С, соответствующее равновесию при контакте с сухим воздухом. На это требовалось 40 мин. Эти значения температуры затвердевания, наблюдающиеся, когда смесь твердой и жидкой кислот находится в равновесии с воздухом, содержащим водяные пары с парциальным давлением 4 6 и 0 5 мм рт. ст., дают возможность экстраполировать температуру затвердевания к значению, соответствующему равновесию с сухим воздухом. Экстраполированное значение температуры было равно 122 373 С, что достаточно хорошо совпадает с экспериментальным значением, полученным в присутствии сухого воздуха, и показывает, что данная кислота не содержит заметного количества бензойного ангидрида. [13]
По ходу данной работы не было обнаружено заметного необратимого разложения бензойной кислоты, если она нагревалась до температур не выше 150 С. Доказательство этому будет приведено ниже. Эту реакцию следует контролировать, так как недопустимо изменение чистоты или прогрессивное возрастание загрязнений, вызывающее соответствующие изменения в температуре затвердевания. По исследованию процесса разложения было поставлено много экспериментов. Если кислота находится в запаянной ампуле, то образующаяся одновременно с ангидридом вода не может уходить из сферы реакции, и реакция поэтому может протекать только до тех пор, пока не установится равновесие. Предполагалось, что для наблюдения воспроизводимой точки плавления кислоту необходимо привести в некоторое состояние равновесия с продуктами ее разложения. Сообразно этому предположению, четыре ампулы поддерживались при температуре выше температуры затвердевания ( за исключением короткого периода, в течение которого производились измерения температуры затвердевания) до тех пор, пока не достигалось равновесие; состояние равновесия характеризовалось постоянством температуры затвердевания кислоты в ампулах. Температура печи примерно на 10 С превышала температуру затвердевания кислоты. Следует заметить, что для достижения равновесия между бензойным ангидридом и водой требуется не менее 10 дней. Небольшой разброс в значениях температуры затвердевания за период до 8 недель связан с растворением в кислоте небольшого количества ангидрида и воды ( около 0 015 мол. Небольшое различие значений температур затвердевания для отдельных ампул в вакууме объясняется, вероятно, различием исходного содержания воды или ангидрида, так как при наполнении ампул и сушке кислоты количество обеих компонент строго не контролировалось. [14]
Страницы: 1