Значение - теплота - сгорание
Cтраница 1
Значения теплоты сгорания относятся к СО, и НгО - рассматриваемым как продукты реакции. [1]
 |
Стандартные значения теплоты образования некоторых распространенных газов. [2] |
Значения теплоты сгорания для ряда газов, жидкостей и твердых веществ приведены в табл. 1.13. Все они определены при нормальном атмосферном давлении и температуре среды, равной 298 К ( 25 С), а также при условии, что сгорание происходит полностью. Необходимо, однако, отметить, что для жидких и твердых горючих веществ значение ДНС представляет собой суммарную теплоту сгорания сконденсированного горючего, а не общую теплоту сгорания летучих веществ. Фактическое тепловыделение при сгорании может быть оценено с помощью закона постоянства сумм тепла ( закон Гесса) при условии, что известен состав продуктов сгорания. [3]
Значение теплоты сгорания, вычисленное по формуле (3.1), соответствует, как правило, погрешности экспериментальных данных. [4]
Значения теплот сгорания примерно на порядок выше значений теплот образования. Поэтому при использовании в расчетах теплот сгорания тепловой эффект реакции получают как небольшую величину в результате разности больших величин. В таких случаях точность расчетов снижается. [5]
Значения теплот сгорания компонентов газа и их теплоемкостей взяты из литературы ( см. сноску на стр. [6]
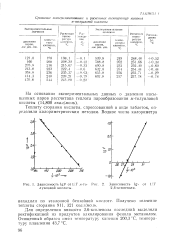 |
Зависимость IgP от 1 / Т. w - то - [ IMAGE ] 2. Зависимость lg -, от 1 / Т лунловой кислоты. 2 6-ксиленола. [7] |
Получено значение теплоты сгорания 911, 321 ккал / моль. [8]
Все значения теплоты сгорания топлив, содержащих влагу и золу, могут колебаться в зависимости от содержания этих примесей, которое часто может быть совершенно случайным. Для научных работ и для классификации топлива необходимо знать теплоту сгорания органической массы угля, а ввиду трудности ее расчета, как об этом говорилось выше, теплоту сгорания горючей массы топлива. Очевидно, что последняя величина является постоянной и характерной для топлива с определенными свойствами. [9]
Получив значение теплоты сгорания янтарной кислоты, хорошо согласующиеся с данными Веркаде, Гартмана и Коопса [161], Кеффлер пришел к выводу о возможности применения янтарной кислоты для этой цели. [10]
 |
Постоянные / 22 Х, Х, Х, У для расчета теплот. [11] |
Сходимость значений теплот сгорания, рассчитанных по упрощенным уравнениям ( 214) - ( 228), с экспериментальными несколько хуже, чем рассчитанных по уравнениям ( 199) - ( 207), однако ошибки расчета и в этом случае близки к ошибкам измерений. [12]
Анализ значений теплот сгорания органических веществ позволяет также делать выводы о стабильности их молекул. [13]
Если из значения теплоты сгорания вычесть значение работы, затраченной на изменение объема при постоянном давлении, то получим теплотворную способность соединения. [14]
Установленные стандартом значения теплоты сгорания, относительной плотности, октанового числа и объемной доли негорючих компонентов поступающего на АГНКС природного газа выбраны с учетом состава природных газов по регионам размещения АГНКС. [15]
Страницы: 1 2 3 4