Значение - стандартная теплота - образование
Cтраница 2
Тепловой эффект химических реакций практически не зависит от давления. Поэтому значения стандартных теплот образования Д 298, помещенные в справочные таблицы, с достаточной точностью могут быть использованы для расчетов тепловых эффектов при различных давлениях. Требуется лишь перейти к заданной температуре с помощью закона Кирхгофа либо с помощью таблиц, содержащих величины ( Hf - Н §) в зависимости от температуры. [16]
Тепловой эффект химических реакций практически не зависит от давления. Поэтому значения стандартных теплот образования АЯ 298, помещенные в справочные таблицы, с достаточной точностью могут быть использованы для расчетов тепловых эффектов при различных давлениях. Требуется лишь перейти к заданной температуре с помощью закона Кирхгофа либо с помощью таблиц, содержащих величины ( Я - Но) в зависимости от температуры. [17]
Энергетически для двуокиси германия наиболее устойчивой является октаэдрическая координация Ge4, так как переход рутиловой формы GeOg в кварцевую сопровождается эндотермическим тепловым эффектом. В соответствии со значением стандартной теплоты образования кварцевой формы Ge02 ( 129.08 ккал / моль) [43 ] пересчет на энтальпию образования кварцевого Ge02 из газообразных одноатомных элементов - теплоту ( энергию) атоми-зации - дает значение - 339 ккал / моль. Сравнение этой величины с аналогичной, теплотой атомизации кварца Si02 - 448 ккал / моль, свидетельствует о меньшей прочности химической связи Ge-О в расчете на одну валентность по сравнению с Si-О: 84.7 и 111.2 ккал / моль, соответственно. [18]
Таким образом, для вычисления констант равновесия необходимо знать теплоту образования и приведенный термодинамический потенциал участвующих в реакции веществ. В табл. 1 приведены значения стандартных теплот образования газообразных летучих галидов. [19]
 |
Стандартная теплота образования некоторых продуктов сгорания. [20] |
В ряде случаев необходимы данные по так называемой низшей теплоте сгорания АН гнизш, которая меньше стандартной на теплоту конденсации образующейся при конденсации воды. Величину низшей теплоты сгорания можно вычислить по соотношению (5.9), используя приведенное в табл. 5.4 значение стандартной теплоты образования газообразной воды. [21]
Силан представляет собой нестабильное соединение, легко разлагающееся на элементы. Разложение его проходит с наименьшей по сравнению с другими соединениями затратой энергии. В табл. 1 приведены значения стандартной теплоты образования для некоторых соединений кремния. [22]
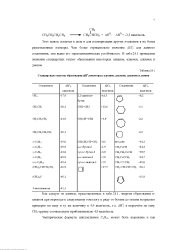 |
Стандартные теплоты образования AH f некоторых алканов, алкенов, алкинов и диенов. [23] |
Этот вывод остается в силе и для изомеризации других н-алканов в их более разветвленные изомеры. Чем более отрицательно значение AH f для данного соединения, тем выше его термодинамическая устойчивость. В табл. 24.1 приведены значения стандартных теплот образования некоторых алканов, алкенов, алкинов и диенов. [24]
Страницы: 1 2