Значение - точка - плавление
Cтраница 1
Значения точек плавления, точек кипения, показателей преломления nf, плотностей d - , теплот плавления, испарения, сжигания и теплот полимеризации, а также пределов взрывоопасностп приведены в основных табл. I и 11 на стр. [1]
Это обусловливает разброс в значениях точек плавления, встречающихся в литературе. [2]
Еще в 1854 г. Томсоном было отмечено, что если значение точки плавления льда известно с достаточной точностью, то с теоретической точки зрения предпочтительнее определять шкалу температур с помощью абсолютного значения точки плавления льда, чем путем отнесения 100 к разнице между значениями точки плавления льда и точки кипения воды. В 1954 г. десятая Генеральная конференция по мерам и весам [1424] пересмотрела определение шкалы температур по Кельвину, приписав значение 273 16 К тройной точке воды; в этом случае точка плавления льда соответствует 273 15 К. [3]
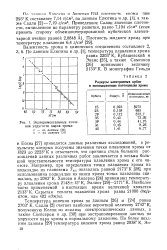 |
Экспериментальные значения упругости паров хрома. [4] |
Есина [27] приводятся данные различных исследований, в результате которых получены значения точки плавления хрома от 1823 до 2223 К и отмечается, что причина столь больших расхождений данных различных работ заключается в весьма большой чувствительности температуры плавления хрома к его чистоте. [5]
На основании изложенного огнеупорность даже для чистых кристаллических веществ отличается от температуры их плавления ( точек плавления); обычно значения огнеупорности выше значений точек плавления. Иногда температуру деформации испытуемых пирамидок допускается определять по показаниям термопар или пирометра. [6]
Еще в 1854 г. Томсоном было отмечено, что если значение точки плавления льда известно с достаточной точностью, то с теоретической точки зрения предпочтительнее определять шкалу температур с помощью абсолютного значения точки плавления льда, чем путем отнесения 100 к разнице между значениями точки плавления льда и точки кипения воды. В 1954 г. десятая Генеральная конференция по мерам и весам [1424] пересмотрела определение шкалы температур по Кельвину, приписав значение 273 16 К тройной точке воды; в этом случае точка плавления льда соответствует 273 15 К. [7]
На значение точек плавления и кипения для характеристики органических веществ указал еще Берцелиус в первом издании своего учебника ( 1810 - 1812), но последовательное практическое применение эти способы получили впервые в работах Шевреля над веществами, выделяемыми из жиров ( 1813), Для однородности препаратов Шеврель ввел фракционную перегонку и перекристаллизацию до достижения постоянных температур соответственно кипения и плавления. Плотностью как характеристикой органических соединений широко пользовались-в первой половине XIX в. [8]
Имеющиеся данные по окиси алюминия представляют особый интерес, так как точка ее плавления часто используется в качестве вторичной постоянной точки. При беглом знакомстве с табл. 2 видно, что имеет место большой разброс значений точек плавления, который может ввести в заблуждение экспериментатора. Существует распространенное мнение, что наиболее точными являются измерения Канольта, который дает наивысшее значение точки плавления. [9]
Комиссия по высокотемпературным исследованиям Международного союза теоретической и прикладной химии в настоящее время решает вопрос о целесообразности субсидирования программы по расширению номенклатуры вторичных постоянных точек. Предполагается, что первая часть программы будет состоять в проведении критических оценок рекомендуемых значений точек плавления выбранных веществ. Использование таких величин, по крайней мере для предварительных оценок, исключит возможность часто имевшего место случайного выбора данных и поможет исследователю наилучшим образом учесть ошибки своих измерений. Вторая часть программы предусматривает разработку экспериментальной методики определения точек плавления выбранных веществ в различных лабораториях стран - участниц Союза. [10]
Гуинн и Питцер [556] измеряли также теплоемкость газообразного 1 2-дибромэтана, однако им не удалось установить параметры для внутреннего вращения, которые приводили бы к результатам статистических расчетов, согласующимся как с энтропией, так и с тепло-емкостями пара. Поэтому приняты экспериментальные значения и использованы оценки для экстраполяции к более высоким температурам. Тиммерманс [1501] приводит восемь значений точки плавления, хорошо согласующихся с данными Питцера [1151], и три значения точки кипения, хорошо согласующиеся при 404 8 К. [11]
Измеренная энтропия соответствует свободному вращению метильной группы. Данные по давлению пара, полученные Херингтоном и Мартином [585], и значения точки плавления и криоскопической энтальпии плавления, установленные Биддискомбом, Коулсоном, Хандли и Херингтоном [127], отлично согласуются между собой. Вторые вириальные коэффициенты и рассчитанные значения энтальпии испарения, установленные Андоном, Коксом, Херингтоном и Мартином [21], а также Коксом и Андоном [287], удовлетворительно согласуются с результатами Скотта и др. Энтальпия сгорания, определенная Коксом, Чолонером и Митэмом [288], приводит к значению АД / 298 ( 0 14 10 ккал / молъ. Нет основания искать причины несоответствия, которое лишь немного превышает сумму экспериментальных ошибок. [12]
Чтобы с помощью уравнения ( I, 65) получить хорошие результаты для большого числа веществ, следует осуществить два сравнения: ( tna) 2m 1 - - ( шОзтИ ( пл) зт-1 - ( пл) 2т и после этого принять среднее значение. Пл) нечетн / ( пл) четн, которая становится ощутимой при распространении ( I, 65) на большое число веществ, является противоположной по знаку для этих двух сравнений. Вместе с тем, указанная рекомендация свидетельствует о том, что в общем случае нельзя отдавать предпочтение какой-либо из двух возможных последовательностей при сравнении значений точек плавления. [13]
Гуинн и Питцер [556] измеряли также теплоемкость газообразного 1 2-дибромэтана, однако им не удалось установить параметры для внутреннего вращения, которые приводили бы к результатам статистических расчетов, согласующимся как с энтропией, так и с тепло-емкостями пара. Поэтому приняты экспериментальные значения и использованы оценки для экстраполяции к более высоким температурам. Тиммерманс [1501] приводит восемь значений точки плавления, хорошо согласующихся с данными Питцера [1151], и три значения точки кипения, хорошо согласующиеся при 404 8 К. [14]
Hv 8 654 ккал / молъ при ТЪ 402 54 К, АЯь 98 10 15 ккал / молъ, S 98 ( Г) 52 07 кал / ( молъ - К), iS 98 ( g) 77 68 кал / ( молъ - К), A. Измеренная энтропия соответствует свободному вращению метальной группы. Данные по давлению пара, полученные Херингтоном и Мартином [585], и значения точки плавления и криоскопической энтальпии плавления, установленные Биддискомбом, Коулсоном, Хандли и Херингтоном [127], отлично согласуются между собой. Вторые вириальные коэффициенты и рассчитанные значения энтальпии испарения, установленные Андоном, Коксом, Херингтоном и Мартином [21], а также Коксом и Андоном [287], удовлетворительно согласуются с результатами Скотта и др. Энтальпия сгорания, определенная Коксом, Чолонером и Митэмом [288], приводит к значению АЯ / 98 ( Г) 14 10 ккал / молъ. Нет основания искать причины несоответствия, которое лишь немного превышает сумму экспериментальных ошибок. [15]
Страницы: 1