Тепловой режим - гетерогенная экзотермическая реакция
Cтраница 1
Тепловой режим гетерогенных экзотермических реакций определяется тремя процессами: переносом реагентов, химической реакцией и отводом тепла. Тепловой режим гомогенных реакций в аппаратах полного смешения, как было показано выше, та же определяется подводом реагентов ( скоростью намыва), скоростью реакции и отводом тепла. Переход от одного режима к другому должен происходить скачкообразно при незначительном изменении условий осуществления процесса, причем эти условия должны зависеть от направления перехода - от низкотемпературного режима к высокотемпературному или наоборот. [1]
Теория теплового режима гетерогенных экзотермических реакций, изучающая наиболее сложный случай, где одновременно существенны и диффузия, и теплопередача. [2]
Другим важным практическим приложением теории теплового режима гетерогенных экзотермических реакций является конструирование каталитических газоанализаторов; в них содержание какого-либо газа в смеси определяется по разогреву поверхности катализатора, где этот газ вступает в каталитическую реакцию. [3]
Наибольший интерес с точки зрения развитой выше теории теплового режима гетерогенных экзотермических реакций представляют процессы сильно экзотермического катализа. Для этих процессов характерно то, что они обычно проводятся на верхнем стационарном тепловом режиме. При этом имеют место большие разности температур между газом и поверхностью катализатора. [4]
Это, на первый взгляд парадоксальное, положение вещей удалось легко объяснить при помощи развитой выше теории теплового режима гетерогенных экзотермических реакций. Очевидно, что на медном катализаторе реакция имеет большую энергию активации, а абсолютная скорость ее невелика. Тогда область устойчивых стационарных тепловых режимов ограничена весьма высокими температурами. Всякая попытка снижения температуры неизбежно приводит к потуханию реакции. [5]
Это, на первый взгляд парадоксальное, положение вещей удалось легко объяснить при помощи развитой выше теории теплового режима гетерогенных экзотермических реакций. Очевидно, что на медном катализаторе реакция имеет большую энергию актива ции, а абсолютная скорость ее невелика. Тогда область устойчивых стационарных тепловых режимов ограничена весьма высокими температурами. Всякая попытка снижения температуры неизбежно приводит к потуханию реакции. [6]
Те же идеи и методы, которые были применены в теории теплового воспламенения для гомогенных реакций, мы применим теперь к вопросу о тепловом режиме гетерогенных экзотермических реакций. Отличие от гомогенных реакций заключается в том, что в этом случае скорость реакции не может уже возрастать неограниченно, вплоть до самых высоких температур. Скорость гетерогенного химического процесса определяется как истинной скоростью химической реакции на поверхности, так и скоростью подвода реагирующих веществ к этой поверхности молекулярной или конвективной диффузией. При низких температурах, пока скорость реакции мала по сравнению со скоростью диффузии ( кинетическая область), суммарная скорость процесса определяется истинной кинетикой на поверхности и экспоненциально возрастает с температурой, согласно закону Аррениуса. Но это возрастание может продолжаться лишь до тех пор, пока скорость реакции не сделается сравнимой со скоростью диффузии. В дальнейшем процесс перейдет в диффузионную область, где скорость его всецело определяется скоростью диффузии и лишь весьма слабо возрастает с температурой. При такой зависимости скорости выделения тепла от температуры и при определенных условиях тепло-отвода возможны три стационарных тепловых режима, из которых средний оказывается неустойчивым, верхний отвечает протеканию реакции в диффузионной, а нижний - в кинетической области. Воспламенение поверхности представляет собой скачкообразный переход от нижнего к верхнему стационарному тепловому режиму. Обратный переход от верхнего теплового режима к нижнему происходит также скачком при критическом условии потухания, не совпадающем с условием воспламенения. [7]
Те же идеи и методы, которые были применены в теории теплового воспламенения для гомогенных реакций, мы применим теперь к вопросу о тепловом режиме гетерогенных экзотермических реакций. Отличие от гомогенных реакций заключается в том, что в этом случае скорость реакции не может уже возрастать неограниченно, вплоть до самых высоких температур. Скорость гетерогенного химического процесса определяется как истинной скоростью химической реакции на поверхности, так и скоростью подвода реагирующих веществ к этой поверхности молекулярной или конвективной диффузией. При низких температурах, пока скорость реакции мала по сравнению со скоростью диффузии ( кинетическая область), суммарная скорость процесса определяется истинной кинетикой на поверхности и экспоненциально возрастает с температурой, согласно закону Аррениуса. Но это возрастание может продолжаться лишь до тех пор, пока скорость реакции не сделается сравнимой со скоростью диффузии. В дальнейшем процесс перейдет в диффузионную область, где скорость его всецело определяется скоростью диффузии и лишь весьма слабо возрастает с температурой. При такой зависимости скорости выделения тепла от температуры и при определенных условиях тепло-отвода возможны три стационарных тепловых режима, из которых средний оказывается неустойчивым, верхний отвечает протеканию реакции в диффузионной, а нижний - в кинетической области. Воспламенение поверхности представляет собой скачкообразный переход от нижнего к верхнему стационарному тепловому режиму. Обратный переход от верхнего теплового режима к нижнему происходит также скачком при критическом условии потухания, не совпадающем с условием воспламенения. [8]
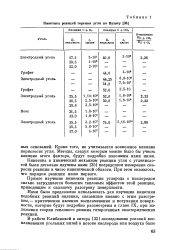 |
Кинетика реакций горения угля по Вулису. [9] |
Нами было предложено использовать для изучения кинетики подобных реакций явления, связанные именно с этим разогревом - критические явления воспламенения и потухания поверхности, которые будут подробно рассмотрены в главе IX, при изложении теории теплового режима гетерогенных экзотермических реакций. [10]
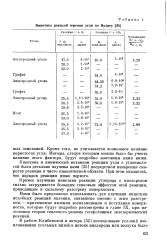 |
Кинетика реакций горения угля по Вулису. [11] |
Нами было предложено использовать для изучения кинетики подобных реакций явления, связанные именно с этим разогревом - критические явления воспламенения и потухания поверхности, которые будут подробно рассмотрены в главе IX, нри изложении теории теплового режима гетерогенных экзотермических реакций. [12]
Нужно, впрочем, отметить, что эта аналогия является полной только в случаях одного реагирующего вещества или стехиомет-рической смеси. Если в реакции участвует несколько веществ, поступающих в реактор, то условие стехиометрии потоков ( II, 42) уже не осуществляется и кинетические уравнения усложняются. Мы ограничимся рассмотрением случаев, когда скорость реакции может быть представлена как функция от одной переменной концентрации. Сюда относятся случаи реакций с участием только одного исходного вещества, стехиометрической исходной смеси, а также случай, когда одно из исходных веществ находится в очень малой концентрации. Таким образом, все результаты предыдущей главы, касающиеся стационарных тепловых режимов, остаются в силе и для реактора идеального смешения. Но в теории теплового режима гетерогенных экзотермических реакций мы не вводили в рассмотрение нестационарные и, в частности, колебательные процессы, что практически оправдано, так как большая тепловая инерция катализатора делает подобные процессы мало вероятными. Напротив, в гомогенном реакторе идеального смешения возможность колебательной неустойчивости ничем не исключается, и мы должны подвергнуть систему ( Х 26) полному анализу на устойчивость. Анализ аналогичен проделанному выше для термокинетической схемы. [13]
Нужно, впрочем, отметить, что эта аналогия является полной только в случаях одного реагирующего вещества или стехиомет -, рической смеси. Если в реакции участвует несколько веществ, поступающих в реактор, то условие стехиометрии потоков ( II, 42) уже не осуществляется и кинетические уравнения усложняются. Мы ограничимся рассмотрением случаев, когда скорость реакции может быть представлена как функция от одной переменной концентрации. Сюда относятся случаи реакций с участием только одного исходного вещества, стехиометрической исходной смеси, а также случай, когда одно из исходных веществ находится в очень малой концентрации. Это вещество можно называть лимитирующим, но в отличие от диффузионной кинетики понятие лимитирующего вещества имеет здесь уже не точный, а приближенный смысл. Таким образом, все результаты предыдущей главы, касающиеся стационарных тепловых режимов, остаются в силе и для реактора идеального смешения. Но в теории теплового режима гетерогенных экзотермических реакций мы не вводили в рассмотрение нестационарные и, в частности, колебательные процессы, что практически оправдано, так как большая тепловая инерция катализатора делает подобные процессы мало вероятными. Напротив, в гомогенном реакторе идеального смешения возможность колебательной неустойчивости ничем не исключается, и мы должны подвергнуть систему ( Х 26) полному анализу на устойчивость. Анализ аналогичен проделанному выше для термокинетической схемы. [14]
Важнейшим техническим процессом гетерогенного горения является горение угля. Процесс осложняется объемными реакциями двоякого рода. С одной стороны, в технике широко используются сорта каменного угля, богатые летучими компонентами. Сгоранию такого топлива предшествует частичное термическое разложение ( коксование) с выделением горючих газов ( углеводородов и водорода), сгорающих в объеме. С другой стороны, даже и при сжигании чистого углерода, кроме углекислого газа С02 на поверхности может образовываться окись углерода СО, догорающая в объеме. Но при достаточном избытке воздуха и высокой температуре поверхности объемные реакции протекают настолько быстро, что заканчиваются в непосредственной близости от поверхности. При этом становится допустимой приближенная трактовка процесса как чисто гетерогенного. Вопрос о гетерогенном горении в такой постановке относится к диффузионной кинетике и тепловому режиму гетерогенных экзотермических реакций и рассматривается нами в соответствующих главах. [15]
Страницы: 1