Значение - квантовое число
Cтраница 3
Как видим, обе операции значения квантового числа т не изменяют. [31]
При I 0 определенной паре значений квантовых чисел пи / соответствует несколько линейно независимых волновых функций. Набор этих функций выбирают одним из двух излагаемых ниже способов. [32]
Угловая составляющая волновой функции определяется значениями квантовых чисел: / - орбитальные и m - магнитные квантовые числа, значения которых обсуждались ранее ( стр. [33]
Угловая составляющая волновой функции определяется значениями квантовых чисел: / - орбитальные и т - магнитные квантовые числа ( см. с. [34]
Эти операторы соответственно повышают или понижают значение квантового числа т для собственных функций оператора углового момента, на которые они действуют. Если собственную функцию углового момента условно записывать при помощи кет-обозначения Дирака ( см. разд. [35]
Радиус атома растет прямо пропорционально квадрату значения квантового числа и для л1, т.е. для невозбужденного атома водорода, г 0 053 нм. [36]
В отсутствие магнитного поля 21 1 значений квантового числа т отвечают одному и тому же значению энергии, но в магнитном поле энергетический уровень W расщепляется на соответствующее число подуровней. Поэтому т и называют магнитным квантовым числом, которое соответствует магнитному квантовому числстаройу квантовой теории. [37]
Электронные термы двухатомных молекул классифицируют по значению квантового числа Л, определяющего величину проекции орбитального момента на ось молекулы. [38]
Систематика электронных термов молекул ведется по значениям квантового числа А, а также квантовых чисел S ий. [39]
Электронные термы двухатомных молекул классифицируют по значению квантового числа Л, определяющего величину проекции орбитального момента на ось молекулы. [40]
Таким образом, оба электрона характеризуются значением квантовых чисел и1, / 0 и. Как видно, принцип Паули, требующий, чтобы электроны в атоме отличались значением хотя бы в отношении одного квантового числа, соблюдается. Ионизационный потенциал атома гелия значительно выше, чем атома водорода, и составляет 2372 дДж / моль что свидетельствует о прочности связи электронов атома гелия с ядром. Закончен первый период и закончен первый уровень. [41]
 |
Различные типы ядер. [42] |
У ядер с / / 2 для значения квантового числа углового момента ядерного спина т /, равные / 2 или - 1 / 2, соответствуют двум возможным ориентациям вектора магнитного момента ядра во внешнем магнитном поле. Значение / 2 отвечает ориентации вектора в направлении магнитного поля, а значение - / 2 - ориентации в противоположном направлении. При 11 mi составляет 1, 0 и - 1, что соответствует ориентациям вектора момента параллельно, перпендикулярно и антипараллельно полю. В отсутствие магнитного поля все ориентации ядерного магнитного момента вырождены, но при наложении поля вырождение снимается. [43]
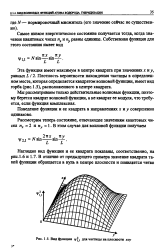 |
Вид функции /., для частицы на плоскости хоу. [44] |
Самое низкое энергетическое состояние получается тогда, когда значения квантовых чисел пх и п равны единице. [45]
Страницы: 1 2 3 4