Значение - энергия - ионизация
Cтраница 2
В табл. 1.1 приведены значения энергий ионизации некоторых атомов. [16]
В табл. 8 приведены значения энергии ионизации некоторых молекул. [17]
В табл. 1.1 приведены значения энергий ионизации некоторых ато-мов. Из нее следует, что наименьшее значение энергии ионизации ( / i) имеют щелочные металлы и что для данного элемента при переходе от одного значения / к другому часто наблюдается резкое изменение энергии. Так, для бора отрыв 4-го и 5-го электронов требует примерно десятикратной ( по сравнению с 1 2 и 3 - м электронами) затраты энергии. В табл. / 1.1 указанные скачки отмечены ступенчатыми линиями. Это непосредственно свидетельствует о группировке электронов в слои. [18]
В табл. 3 приведены значения энергий ионизации некоторых атомов. Из нее следует, что наименьшее значение 1 имеют щелочные металлы и что для данного элемента при переходе от одного значения / к другому наблюдается резкое изменение потенциала ионизации. [19]
В табл. 14 приведены значения энергии ионизации /, затрачиваемой на отрыв первого ( валентного), затем второго и последующих электронов от электронейтрального атома. Из приведенных данных видно, что энергия ионизации валентных электронов значительно меньше, чем электронов, входящих в состав достроенных электронных слоев. Электроны могут не только отрываться, но и присоединяться к атомам. Сродством к электрону Е называется количество энергии, которое выделяется при присоединении электрона к нейтральному атому или к отрицательно заряженному иону. Сродство к электрону, так же как и ионизационные потенциалы, выражается в электрон-вольтах на атом или килоджоулях на килограм-атом. [20]
В табл. 1.1 приведены значения энергий ионизации некоторых атомов. Наименьшее значение энергии ионизации ( / i) имеют щелочные металлы. У элементов при переходе от одного значения I к другому часто наблюдается резкое изменение энергии. Так, для атома бора отрыв 4-го и 5-го электронов требует примерно десятикратной ( по сравнению с 1 -, 2 - и 3 - м электронами) затраты энергии. В табл. 1.1 указанные скачки отмечены ступенчатыми линиями. Данная закономерность непосредственно свидетельствует о группировке электронов в слои. [21]
В табл. 12 даны значения энергии ионизации некоторых атомов. [22]
В табл. 5 приведены значения энергий ионизации для некоторых атомов. [23]
В приводимой таблице даны значения энергии ионизации в электрон-вольтах для некоторых атомов. Отметим, что разность потенциалов, которую должен пройти свободный электрон для приобретения энергии ионизации, называют ионизационным потенциалом атома. [24]
В табл. 25 приведены значения энергий ионизации, атомов примеси при фото-и термоионизации. Обращает на себя внимание тот факт, что энергия фотоионизации несколько больше энергии термической ионизации. [25]
В табл. 5 приведены значения энергий ионизации для некоторых атомо. [26]
В табл. 5 приведены значения энергий ионизации для некоторых атомов. [27]
В табл. 1.1 приведены значения энергий ионизации некоторых атомов. Наименьшее значение энергии ионизации ( А) имеют щелочные металлы. У элементов при переходе от одного значения / к другому часто наблюдается резкое изменение энергии. Так, для атома бора отрыв 4-го и 5-го электронов требует примерно десятикратной ( по сравнению с 1 -, 2 - и 3 - м электронами) затраты энергии. В табл. 1.1 указанные скачки отмечены ступенчатыми линиями. Данная закономерность непосредственно свидетельствует о группировке электронов в слои. [28]
В табл. 3 приведены значения энергий ионизации некоторых атомов. Из нее следует, что наименьшее значение / 4 имеют щелочные металлы и что для данного элемента при переходе от одного значения / к другому Часто наблюдается резкое изменение потенциала ионизации. Так, для бора отрыв 4-го и 5-го электронов требует примерно десятикратной ( по сравнению с 1, 2 и 3 - м электронами) затраты энергии. Последнее обстоятельство непосредственно свидетельствует о группировке электронов в слои. В табл. 3 указанные скачки отмечены ступенчатыми линиями. [29]
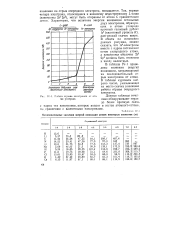 |
Последовательные значения энергий ионизации атомов некоторых элементов ( эв. [30] |
Страницы: 1 2 3 4