Значение - энергия - гидратация
Cтраница 2
 |
Растянутые и изогнутые водородные связи. [16] |
Электростатическая концепция ограничивается главным образом тем, что экспериментальные данные всегда отражают одновременное воздействие катионов и анионов, так как невозможно измерить независимо энергию их гидратации. Данные для отдельных ионов можно вычислить лишь при подходящих предположениях, однако эти предположения спорны. Об этом свидетельствуют значительные различия в значениях энергии гидратации, вычисленных с использованием ряда возможных предположений, базирующихся по существу на электростатических эффектах, вычисленных из соответствующих экспериментальных данных. [17]
После ознакомления с основными методами расчета, применяемыми при изучении энергетики процесса гидратации, интересно сопоставить результаты, полученные при помощи этих методов. Такое сопоставление позволяет судить, во-первых, о величинах теплот и энергий гидратации, и, во-вторых, о том, насколько результаты различных авторов согласуются между собой. В табл. 14 приведены значения теплот гидратации и в табл. 15 - значения энергий гидратации. Наряду с данными, полученными по описанным ранее методам, включены также результаты расчетов другими методами. В методе Фаянса используются циклы, связанные с применением водородного и амальгамного калиевого электродов и рассчитываются соответственно теплоты гидратации протона и иона калия. [18]
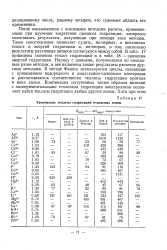 |
Химические теплоты гидратации отдельных ионов. [19] |
После ознакомления с основными методами расчета, применяемыми при изучении энергетики процесса гидратации, интересно сопоставить результаты, полученные при помощи этих методов. Такое сопоставление позволяет судить, во-первых, о величинах теплот и энергий гидратации и, во-вторых, о том, насколько результаты различных авторов согласуются между собой. В табл. 17 приведены значения теплот гидратации и в табл. 18 - значения энергий гидратации. Наряду с данными, полученными по описанным ранее методам, в нее включены также результаты расчетов другими методами. В методе Фаянса используются циклы, связанные с применением водородного и амальгамно-калиевого электродов и рассчитываются соответственно теплоты гидратации протона и иона калия. Комбинация полученных таким образом величин с экспериментальными теплотами гидратации электролитов позволяет найти теплоты гидратации любых других ионов. [20]
При таком допущении энергия активации должна быть функцией энергии гидратации ионов и работы их выхода из металла, возрастая с увеличением разности между ними. Однако имеющиеся данные ( см. табл. 22.3) не подтверждают такого предположения: так, для цинка и никеля значения энергии гидратации и работы выхода почти одинаковы, но цинк выделяется со значительно меньшим перенапряжением, чем никель. Это отнюдь не означает, что прочность ионов в растворе и в металле не играет никакой роли, ее просто нельзя учесть подобным примитивным способом. [21]
Следует учесть, что значения АЯЙ, вычисленные по уравнению ( 27), являются приближенными, так как уравнение Борна основано на простой электростатической модели, в которой ион находится в сплошной среде с постоянной диэлектрической проницаемостью, тогда как в действительности необходимо учитывать истинную молекулярную структуру среды. Тем не менее значения теплот гидратации комплексных ионов и лигандов, вычисленные по уравнению ( 27), можно использовать для выявления закономерностей в энергиях гидратации или величинах А / / / [ уравнение ( 18) ] для рядов ионов металлов. Таким образом, теплоты гидратации хорошо известны для ионов металлов, сравнительно мало изучены для лигандов и почти неизвестны для большинства комплексов металлов. Важно помнить, что все значения энергии гидратации, определенные экспериментально, выражены в относительной шкале, где тепловой эффект водородного полуэлемента [ уравнение ( 23) ] принят равным нулю. [22]
Чем выше эффективная напряженность поля, тем слабее кислота или основание [83, 84] Следовательно, бензилтриметил-аммониевые группы обычных сильноосновных анионитов обладают слишком слабым полем, чтобы ряды селективности для этих анионитов могли определяться электростатическим взаимодействием. Так, разность полных электростатических энергий для анионов хлора и перхлората составляет только 10 4 ккал / молъ, в то время как разность энергий гидратации этих ионов равна 30 5 ккал / молъ. Если наши соображения верны, то для анионитов с гораздо более слабыми основными группами, чем группа бензилтриметиламмония, энергия электростатического взаимодействия должна быть значительно больше. Разности этих энергий также должны резко возрасти. Тогда с ростом напряженности поля будет повышаться роль электростатического взаимодействия в явлениях селективности и для наиболее сильных полей мы должны получить ряд С1 - Вг - 1 - СЮ, который может быть назван полностью обращенным рядом, так как порядок анионов в нем в точности противоположен порядку, которого следовало бы ожидать на основании значений энергии гидратации. [23]
Чем выше эффективная напряженность поля, тем слабее кислота или основание [83, 84] Следовательно, бензилтриметил-аммониевые группы обычных сильноосновных анионитов обладают слишком слабым полем, чтобы ряды селективности для этих анионитов могли определяться электростатическим взаимодействием. Так, разность полных электростатических энергий для анионов хлора и перхлората составляет только 10 4 ккал / молъ, в то время как разность энергий гидратации этих ионов равна 30 5 ккал / молъ. Если наши соображения верны, то для анионитов с гораздо более слабыми основными группами, чем группа бензилтриметил аммония, энергия электростатического взаимодействия должна быть значительно больше. Разности этих энергий также должны резко возрасти. Тогда с ростом напряженности поля будет повышаться роль электростатического взаимодействия в явлениях селективности и для наиболее сильных полей мы должны получить ряд С1 - Вг - 1 - СЮ 7, который может быть назван полностью обращенным рядом, так как порядок анионов в нем в точности противоположен порядку, которого следовало бы ожидать на основании значений энергии гидратации. [24]
Страницы: 1 2